题目内容
某酸性溶液中只含N
、Cl-、H+、OH-四种离子,下列说法正确的是( )
| H | + 4 |
分析:A.如盐酸过量,可存在c(C1-)>c(H+)>c(NH4+)>c(OH-);
B.等物质的量浓度、等体积的盐酸和氨水混合,溶液可呈酸性;
C.pH=3的盐酸与pH=11的氨水等体积混合,氨水过量,溶液呈碱性;
D.溶液电荷不守恒.
B.等物质的量浓度、等体积的盐酸和氨水混合,溶液可呈酸性;
C.pH=3的盐酸与pH=11的氨水等体积混合,氨水过量,溶液呈碱性;
D.溶液电荷不守恒.
解答:解:A.如盐酸过量较多,可存在c(C1-)>c(H+)>c(NH4+)>c(OH-),故A正确;
B.等物质的量浓度、等体积的盐酸和氨水混合,恰好生成NH4Cl,为强酸弱碱盐,溶液呈酸性,故B错误;
C.pH=3的盐酸与pH=11的氨水等体积混合,氨水过量,溶液呈碱性,故C错误;
D.溶液电荷不守恒,如c(H+)>c(OH-),应有c(C1-)>c(NH4+),或c(OH-)>c(H+),应有c(NH4+)>c(C1-),故D错误,
故选A.
B.等物质的量浓度、等体积的盐酸和氨水混合,恰好生成NH4Cl,为强酸弱碱盐,溶液呈酸性,故B错误;
C.pH=3的盐酸与pH=11的氨水等体积混合,氨水过量,溶液呈碱性,故C错误;
D.溶液电荷不守恒,如c(H+)>c(OH-),应有c(C1-)>c(NH4+),或c(OH-)>c(H+),应有c(NH4+)>c(C1-),故D错误,
故选A.
点评:题考查离子浓度大小比较,题目难度中等,本题注意一水合氨为弱电解质的特点以及从溶液电中性的角度分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
|
下列溶液中各微粒的浓度关系一定正确的是 | |
| [ ] | |
A. |
物质的量浓度相同的4种溶液①CH3COONa;②NaNO3;③Na2CO3;④NaOH,pH的大小顺序是:④>③>①>② |
B. |
在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO |
C. |
25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1∶1 |
D. |
某酸性溶液中只含NH c(Cl-)>c(NH |
下列溶液中各微粒的浓度关系一定正确的是( )
A.某酸性溶液中只含NH 、Cl-、H+、OH-四种离子,溶液中一定存在: 、Cl-、H+、OH-四种离子,溶液中一定存在:c(Cl-)>c(NH  )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
| B.物质的量浓度相同的4种溶液:①CH3COONa;②NaNO3;③Na2CO3;④NaOH, pH的大小顺序是:④>③>①>② |
C.在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO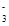 )+c(OH-)+c(CO )+c(OH-)+c(CO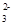 ) ) |
| D.25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1∶1 |
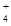 、Cl-、H+、OH-四种离子,溶液中一定存在:
、Cl-、H+、OH-四种离子,溶液中一定存在: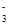 )+c(OH-)+c(CO
)+c(OH-)+c(CO )
)