题目内容
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如图所示,其中不正确的是
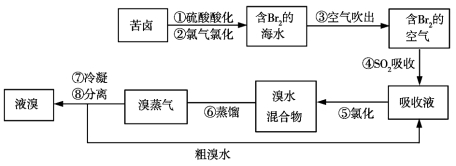
A.溴在周期表中位于第四周期第ⅦA族
B.步骤③说明溴具有挥发性
C.步骤④的离子方程式为Br2+SO2+H2O![]() 2H++2Br-+S
2H++2Br-+S
D.步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物可用分液漏斗分离
【答案】C
【解析】
试题分析:A.溴的原子序数为35,原子结构中有4个电子层,最外层电子数为7,所以溴在周期表中位于四周期VIIA族,A正确;B.空气可用吹出溴,则步骤③说明溴具有挥发性,B正确;C.步骤④发生SO2+Br2+2H2O=2HBr+H2SO4,离子反应为Br2+SO2+2H2O=4H++2Br-+SO42-,C错误;D.实现大量液溴和少量溴水分离的方法是分液法,采用的仪器为分液漏斗,操作时下层液体必须从下口流出,上层液体从上口倒出,D正确,答案选C。

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】某化学小组探究酸性条件下N03 -、S042-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。 (忽略氧气对反应的影响)
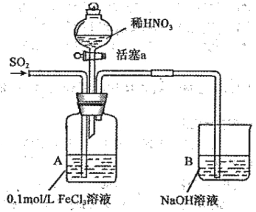
实验记录如下:
实验 序号 | 实验操作 | '...!实验现象 |
I | 向A装置中通入一段时间的SO2气体。. | A中g色溶液最终变为浅绿色。 |
II | 取出少量A装置中的溶破,先加入 KSCN溶液,再加入BaCl2溶液。 | 加人KSCN溶液后溶液不变色;再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A 中,关闭活塞a。 | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加人KSCN 溶液。 | 溶液变为红色。 |
请回答下列问题:
(1)写出A装置中通人二氧化硫气体发生反应的离子方程式 。
(2)实验II中发生反应的离子方程式是 。
(3)实验III中,浅绿色溶液变为棕色的原因是 。(用语言叙述)。
(4)实验IV若往A中通入人空气,液面上方的现象是 。
(5)综合上述实验得岀的结论是:在酸性条件下,氧化性强弱顺序为 。