��Ŀ����
��ͼ��ú������ҵ����һ���֣���������ѧ֪ʶ������������⣺
(1)��֪�ò�ҵ����ij��Ӧ��ƽ�����ʽΪ��K��
������Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
��֪��һ���¶��£���ͬһƽ����ϵ�и���Ӧ��ƽ�ⳣ�����£�
C(s)+CO2(g) 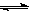 2CO(g)��K1
2CO(g)��K1
CO(g)+H2O(g) 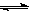 H2(g)+CO2(g)��K2
H2(g)+CO2(g)��K2
C(s)+H2O(g) 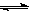 CO(g)+H2(g)��K3
CO(g)+H2(g)��K3
��K1��K2��K3֮��Ĺ�ϵΪ ��
(2)ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⡣��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���������·�Ӧ��CO(g)+H2O(g) H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
(3)���ڷ�ӦN2O4(g)
 2NO2(g)����H=Q��Q>0�������¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ�������� ������
2NO2(g)����H=Q��Q>0�������¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ�������� ������
A�����ֲ�ͬ���¶ȱȽϣ�T1 > T2
B��A��C����ķ�Ӧ���ʣ�A<C
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���ʵ��
(4)����ͼ������NH3����ԭ����������һ��������ͨ�����ֲ�ͬ�����������ݳ������е������ﺬ�����Ӷ�ȷ�������ѵ��ʣ���Ӧԭ��Ϊ��NO(g) + NO2(g) + 2NH3(g)
 2N2(g) + 3H2O(g)
2N2(g) + 3H2O(g)
 ����˵����ȷ���ǣ�ע���ѵ��ʼ���������ת���ʣ�
����˵����ȷ���ǣ�ע���ѵ��ʼ���������ת���ʣ�A��������Ӧ������ӦΪ���ȷ�Ӧ
B����ͬ�����£��ı�ѹǿ���ѵ���û��Ӱ��
C�����ߢ١�����ߵ��ʾ��ʱƽ��ת�������
D�������١��ڷֱ��ʺ���250���450�������ѵ�
(1)��2�֣�C��s��+H2O��g�� CO��g��+H2��g�� K3=K1?K2
CO��g��+H2��g�� K3=K1?K2
(2)��2�֣����ȣ�75% ����1�֣�
(3)��2�֣�B��D ��һ��1�֣���һ����2�֣�
(4)��2�֣�D
����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д���16�֣���ͼ��ú������ҵ����һ���֣���������ѧ֪ʶ������������⣺
��1���ò�ҵ���кϳɰ��ķ�Ӧ�ڽϵ������ܷ��Է����У� ��
��2����֪�ò�ҵ����ij��Ӧ��ƽ�����ʽΪ��
������Ӧ�Ļ�ѧ��ӦΪ�� ��
��3����֪��һ���¶��£�����Ӧ��ƽ�ⳣ�����£�
C��s��+CO2��g�� 2CO��g����K1
CO��g��+H2O��g H2��g��+CO2��g���� K2
C��s��+H2O��g�� CO��g��+H2��g�� ��K3
��K1��K2��K3֮��Ĺ�ϵ�ǣ� ��
��4��ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⡣��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO(g)+H2O(g) H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
�÷�Ӧ������Ӧ������ ��Ӧ������ȡ����ȡ���������500��ʱ���У�����ʼʱCO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol/L���ڸ������£�CO��ƽ��ת����Ϊ�� ��
��5����ͼ�п��������������������ᣬ�˹������漰���������NO��NO2��N2O4�ȡ���֪NO2��N2O4�Ľṹʽ�ֱ�����
����֪N��N������Ϊ167kJ��mol��1��NO2�е������ļ���Ϊ466kJ��mol��1��N2O4�е������ļ���Ϊ438.5kJ��mol��1����д��NO2ת��ΪN2O4���Ȼ�ѧ����ʽΪ ��
�Է�ӦN2O4(g)2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��
����˵����ȷ���ǡ���������
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���
��6����������ҵ���м״�Ϊȼ���Ƴ�ȼ�ϵ�أ���д�����������ؽ����иõ�صĸ�����Ӧʽ ��
��13�֣�ʵʩ�Լ�����Դ�˷Ѻͽ��ͷ����ŷ�Ϊ�������ݵĽ��ܼ������ߣ���Ӧ��ȫ���������⡢������Դ��Լ�͡������Ѻ������ı�Ȼѡ������ҵ�ķ�չ������Ϲ��ҽ��ܼ��ŵ�����Ҫ����ͼ��ú������ҵ����һ���֣���������ѧ֪ʶ������������⣺
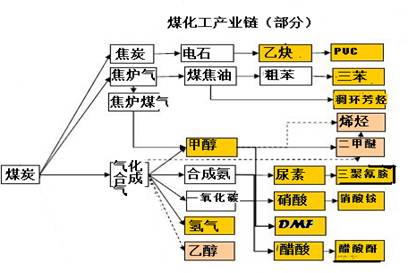
��1���ò�ҵ�������ڸ��нγ������ڵ��������Է����еķ�Ӧ�ǣ�
��2����֪�ò�ҵ����ij��Ӧ��ƽ�����ʽΪ��
������Ӧ�Ļ�ѧ��ӦΪ��
��3����֪��һ���¶��£�
C��s��+CO2��g��  2CO��g��ƽ�ⳣ��K1��
2CO��g��ƽ�ⳣ��K1��
CO��g��+H2O��g  H2��g��+CO2��g��ƽ�ⳣ��K2��
H2��g��+CO2��g��ƽ�ⳣ��K2��
C��s��+H2O��g�� CO��g��+H2��g�� ƽ�ⳣ��K3��
CO��g��+H2��g�� ƽ�ⳣ��K3��
��K1��K2��K3֮��Ĺ�ϵ�ǣ� ��
��4��ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⡣��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO(g)+H2O(g)  H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���±���ʾ��
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���±���ʾ��
|
�¶�/�� |
400 |
500 |
800 |
|
ƽ�ⳣ��K |
9.94 |
9 |
1 |
�÷�Ӧ������Ӧ������ ��Ӧ������ȡ����ȡ���������500��ʱ���У�����ʼʱCO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol/L���ڸ������£�CO��ƽ��ת����Ϊ�� ��
��5������ͼ���������������������ᣬ�˹������漰���������NO��NO2��N2O4�ȡ��Է�ӦN2O4(g)  2NO2(g) ��H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ������������������
2NO2(g) ��H��0���¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ������������������
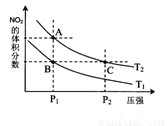
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���
E��A��C����Ļ�ѧƽ�ⳣ����A��C
��6��0.2mol/L��NaOH��0.4mol/L��������ҵ����һ��Ʒ�����������Һ�������Ϻ���Һ�и����ӵ����ʵ���Ũ�ȴӴ�С��˳���� ��
��16�֣���ͼ��ú������ҵ����һ���֣���������ѧ֪ʶ������������⣺

��1���ò�ҵ���кϳɰ��ķ�Ӧ�ڽϵ������ܷ��Է����У� ��
��2����֪�ò�ҵ����ij��Ӧ��ƽ�����ʽΪ��
������Ӧ�Ļ�ѧ��ӦΪ�� ��
��3����֪��һ���¶��£�����Ӧ��ƽ�ⳣ�����£�
C��s��+CO2��g��  2CO��g����K1
2CO��g����K1
CO��g��+H2O��g  H2��g��+CO2��g���� K2
H2��g��+CO2��g���� K2
C��s��+H2O��g�� CO��g��+H2��g�� ��K3
CO��g��+H2��g�� ��K3
��K1��K2��K3֮��Ĺ�ϵ�ǣ� ��
��4��ú����ͨ��ͨ���о���ͬ�¶���ƽ�ⳣ���Խ������ʵ�����⡣��֪�������һ����̼��ˮ�������뷴Ӧ��ʱ���ᷢ�����·�Ӧ��CO(g)+H2O(g)  H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
|
�¶�/�� |
400 |
500 |
800 |
|
ƽ�ⳣ��K |
9.94 |
9 |
1 |
�÷�Ӧ������Ӧ������ ��Ӧ������ȡ����ȡ���������500��ʱ���У�����ʼʱCO��H2O����ʼŨ�Ⱦ�Ϊ0.020mol/L���ڸ������£�CO��ƽ��ת����Ϊ�� ��
��5����ͼ�п��������������������ᣬ�˹������漰���������NO��NO2��N2O4�ȡ���֪NO2��N2O4�Ľṹʽ�ֱ��� ��
�� ����֪N��N������Ϊ167kJ��mol��1��NO2�е������ļ���Ϊ466kJ��mol��1��N2O4�е������ļ���Ϊ438.5kJ��mol��1����д��NO2ת��ΪN2O4���Ȼ�ѧ����ʽΪ
��
����֪N��N������Ϊ167kJ��mol��1��NO2�е������ļ���Ϊ466kJ��mol��1��N2O4�е������ļ���Ϊ438.5kJ��mol��1����д��NO2ת��ΪN2O4���Ȼ�ѧ����ʽΪ
��
�Է�ӦN2O4(g)
 2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��
2NO2(g)�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ��

����˵����ȷ���ǡ���������
A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C��B��C����������ƽ����Է���������B��C
D����״̬B��״̬A�������ü��ȵķ���
��6����������ҵ���м״�Ϊȼ���Ƴ�ȼ�ϵ�أ���д�����������ؽ����иõ�صĸ�����Ӧʽ ��



 �� �÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
�� �÷�Ӧƽ�ⳣ�����¶ȵı仯���£�


 �����ĵ缫��ӦʽΪ_______��
�����ĵ缫��ӦʽΪ_______��
 �� CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ�CaCl2��Һ��
�� CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ�CaCl2��Һ�� ��Na2CO3��Һ�������ϣ������ɳ���ʱԭCaCl2��Һ����СŨ��Ϊ_______��
��Na2CO3��Һ�������ϣ������ɳ���ʱԭCaCl2��Һ����СŨ��Ϊ_______��
 2C0(g) ��H>O��K1
��
��
2C0(g) ��H>O��K1
��
��

