题目内容
11.87g金属锡跟l00mL l2mol/L HNO3共热一段时间,完全反应后测得溶液中的c(H+)=8mol/L,溶液的体积仍为l00mL,放出的气体在标准状况下为8.96L.由此推断氧化产物可能是( )A.Sn(NO3)2
B.SnO2?4H2O
C.Sn(NO3)4
D.Sn(NO3)2和Sn(NO3)4
【答案】分析:根据l2mol/LHNO3为浓硝酸,完全反应后测得溶液中的c(H+)=8mol/L,则浓硝酸有剩余,即锡与浓硝酸反应生成NO2,利用得失电子守恒来分析金属锡被氧化后元素的化合价.
解答:解:11.87g金属锡的物质的量为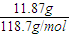 =0.1mol,
=0.1mol,
l2mol/L HNO3为浓硝酸,完全反应后测得溶液中的c(H+)=8mol/L,则浓硝酸有剩余,即锡与浓硝酸反应生成NO2,
则标准状况下NO2的物质的量为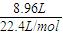 =0.4mol,
=0.4mol,
设金属锡被氧化后元素的化合价为x,
由电子守恒可知,
0.1mol×(x-0)=0.4mol×(5-4),
解得x=+4,
又溶液中c(H+)=8mol/L,而c(NO3-)=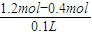 =8mol/L,根据溶液电中性可判断溶液中不存在Sn(NO3)4,
=8mol/L,根据溶液电中性可判断溶液中不存在Sn(NO3)4,
故选B.
点评:本题考查氧化还原反应中电子守恒的计算,明确l2mol/L的HNO3为浓硝酸及电子守恒、溶液呈电中性是解答本题的关键,本题易错选C.
解答:解:11.87g金属锡的物质的量为
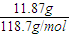 =0.1mol,
=0.1mol,l2mol/L HNO3为浓硝酸,完全反应后测得溶液中的c(H+)=8mol/L,则浓硝酸有剩余,即锡与浓硝酸反应生成NO2,
则标准状况下NO2的物质的量为
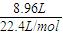 =0.4mol,
=0.4mol,设金属锡被氧化后元素的化合价为x,
由电子守恒可知,
0.1mol×(x-0)=0.4mol×(5-4),
解得x=+4,
又溶液中c(H+)=8mol/L,而c(NO3-)=
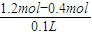 =8mol/L,根据溶液电中性可判断溶液中不存在Sn(NO3)4,
=8mol/L,根据溶液电中性可判断溶液中不存在Sn(NO3)4,故选B.
点评:本题考查氧化还原反应中电子守恒的计算,明确l2mol/L的HNO3为浓硝酸及电子守恒、溶液呈电中性是解答本题的关键,本题易错选C.

练习册系列答案
相关题目
