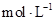题目内容
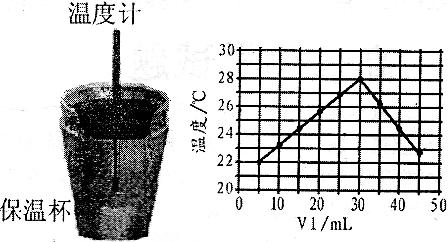
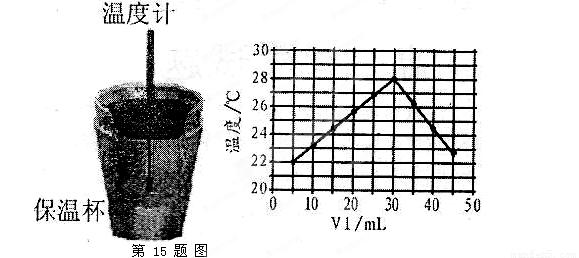
某化学学习小组在实验室里利用图1装置测定中和反应中的热效应.实验时将V1mL 1.0 mol.L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如图2所示(实验中始终保持V1+V2=50mL).
据此请回答下列问题:
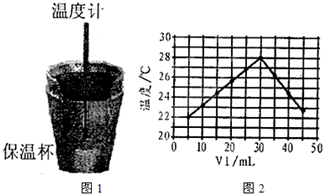
(1)从实验装置上看,图1中尚缺少的一种玻璃用品是
(2)保温杯的作用是
(3)某同学根据所得数据,提出了以下观点,其中正确的是
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.该实验表明有水生成的反应都是放热反应
(4)利用图中所给数据,可测得NaOH溶液的浓度约为
(5)除了使用保温杯外,为了保证实验成功,还要注意哪些问题(说出1点即可)
据此请回答下列问题:

(1)从实验装置上看,图1中尚缺少的一种玻璃用品是
环形玻璃搅拌器
环形玻璃搅拌器
.(2)保温杯的作用是
保温、隔热、减少实验过程中的热量散失
保温、隔热、减少实验过程中的热量散失
.(3)某同学根据所得数据,提出了以下观点,其中正确的是
B
B
.A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.该实验表明有水生成的反应都是放热反应
(4)利用图中所给数据,可测得NaOH溶液的浓度约为
1.5
1.5
mol?L-1(5)除了使用保温杯外,为了保证实验成功,还要注意哪些问题(说出1点即可)
迅速混合,减少热量损失,酸或碱一次性倒入
迅速混合,减少热量损失,酸或碱一次性倒入
.分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败为保温;
(3)A.由图可知,未混合温度为20℃;
B.该实验为中和反应,放出热;
C.有水生成的反应可能为吸热反应,如氢气还原CuO;
(4)根据c1V1=c2V2计算;
(5)迅速混合,减少热量损失,酸或碱一次性倒入,正确的测定最高温度等.
(2)中和热测定实验成败为保温;
(3)A.由图可知,未混合温度为20℃;
B.该实验为中和反应,放出热;
C.有水生成的反应可能为吸热反应,如氢气还原CuO;
(4)根据c1V1=c2V2计算;
(5)迅速混合,减少热量损失,酸或碱一次性倒入,正确的测定最高温度等.
解答:解:(1)根据量热计的构造来判断该装置的缺少仪器为环形玻璃搅拌器,故答案为:环形玻璃搅拌器;
(2)中和热测定实验成败为保温,其作用是保温、隔热、减少实验过程中的热量散失,故答案为:保温、隔热、减少实验过程中的热量散失;
(3)A.由图可知,未混合温度为20℃,故A错误;
B.该实验为中和反应,放出热,则化学能转化为热能,故B正确;
C.有水生成的反应可能为吸热反应,如氢气还原CuO,则一个反应不能得出普遍结论,故C错误;
故答案为:B;
(4)根据c1V1=c2V2可知,由V1+V2=50mL可知,盐酸为30mL,恰好消耗的氢氧化钠溶液的体积为20mL,
则n=1mol/L×0.03L=0.03mol,所以NaOH的浓度是
=1.5mol/L,故答案为:1.5;
(5)迅速混合,减少热量损失,酸或碱一次性倒入,正确的测定最高温度等可保证实验成功,故答案为:迅速混合,减少热量损失,酸或碱一次性倒入.
(2)中和热测定实验成败为保温,其作用是保温、隔热、减少实验过程中的热量散失,故答案为:保温、隔热、减少实验过程中的热量散失;
(3)A.由图可知,未混合温度为20℃,故A错误;
B.该实验为中和反应,放出热,则化学能转化为热能,故B正确;
C.有水生成的反应可能为吸热反应,如氢气还原CuO,则一个反应不能得出普遍结论,故C错误;
故答案为:B;
(4)根据c1V1=c2V2可知,由V1+V2=50mL可知,盐酸为30mL,恰好消耗的氢氧化钠溶液的体积为20mL,
则n=1mol/L×0.03L=0.03mol,所以NaOH的浓度是
| 0.03mol |
| 0.02L |
(5)迅速混合,减少热量损失,酸或碱一次性倒入,正确的测定最高温度等可保证实验成功,故答案为:迅速混合,减少热量损失,酸或碱一次性倒入.
点评:本题考查中和热测定、酸碱中和滴定,明确实验的原理、步骤、注意事项、数据处理等即可解答,题目难度中等.

练习册系列答案
相关题目
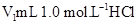 溶液和
溶液和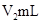 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持
未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持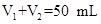 )。
)。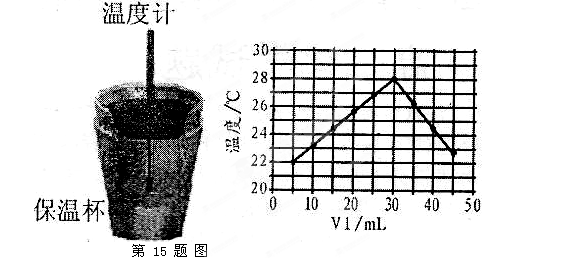 (1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。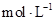
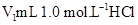 溶液和
溶液和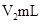 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持
未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持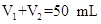 )。
)。 (1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。