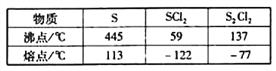
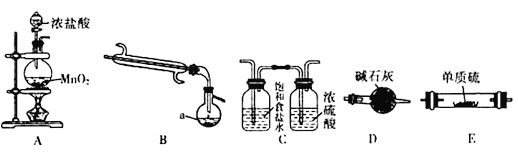
题目内容
【题目】现有一种简单可行的测定阿伏伽德罗常数的方法,具体步骤为:①将固体NaCl细粒干燥后,准确称取m克NaCl固体并转移到定容仪器A中;②用滴定管向仪器A中滴加苯,不断振荡,继续加苯至A仪器的刻度处计算出NaCl固体的体积为Vml,请回答下列问题:
(1)步骤①中A仪器最好用______________
A、量筒 B、烧杯 C、容量瓶 D、试管
(2)步骤②中用酸式滴定管还是碱式滴定管______________理由是___________________
(3)能否用水代替苯?_______,理由是_______________________。
(4)已知NaCl晶体中,靠的最近的钠离子与氯离子间的平均距离为acm,用上述方法测得的阿伏伽德罗常数的表达式为:_________________________
【答案】 C 酸式滴定管 苯是优良的有机溶剂,会溶解碱式滴定管下端的橡胶管。 不可以 氯化钠溶于水后的体积小于水的体积与氯化钠固体的体积之和,导致测量氯化钠的体积不准确。 ![]()
【解析】试题分析:(1)定容仪器是容量瓶;(2)苯是有机溶剂,能腐蚀橡胶;(3). 氯化钠溶于水后的体积小于水的体积与氯化钠固体的体积之和;(4)根据NaCl的密度和晶体的体积计算出一个NaCl晶胞的质量,根据1molNaCl的质量、摩尔质量和阿伏加德罗常数的关系计算阿伏加德罗常数;
解析:(1)定容容器为容量瓶,具有一定体积并便于振荡;苯具有腐蚀性,易腐蚀碱式滴定管中的橡皮管,只能用酸式滴定管;(2)氯化钠溶于水后的体积小于水的体积与氯化钠固体的体积之和,导致测量氯化钠的体积不准确,所以不能用水代替苯;
(3)NaCl的密度为![]() g/cm3,
g/cm3,
NaCl晶胞的体积为(2a)3cm3,
则NaCl晶胞的质量为
![]() ×(2a)3g,一个NaCl晶胞含4个“NaCl”,而每个“NaCl”的质量为
×(2a)3g,一个NaCl晶胞含4个“NaCl”,而每个“NaCl”的质量为![]() =
=![]() g,故:
g,故:![]() ×(2a)3=4×
×(2a)3=4×![]() ,
,
即NA=![]() 。
。

 能考试全能100分系列答案
能考试全能100分系列答案【题目】已知某化学反应的平衡常数表达式为K=![]() ,在不同的温度下该反应的
,在不同的温度下该反应的
平衡常数如表所示
t ℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述正确的是( )
A. 该反应的化学方程式是: H2(g)+CO2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)
B. 上述反应的正反应是吸热反应
C. 如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,如果此时测得CO2为0.5 mol,则该反应达到平衡状态
D. 某温度下,如果平衡常数符合下列关系式: ![]() =
=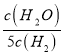 ,则此时温度700℃
,则此时温度700℃