题目内容
在2 L的密闭容器中发生反应:2SO2 + O2 2SO3,如果2
min内SO2的量由12 mol
2SO3,如果2
min内SO2的量由12 mol
下降为4 mol,则下列说法正确的是
A.用SO2的浓度变化表示的反应速率为4 mol/(L·min)
B.用O2的浓度变化表示的反应速率为2 mol/(L·min)
C.增大压强,正反应速率增大,逆反应速率减小
D.升高温度,正反应速率和逆反应速率都增大
D
【解析】

 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是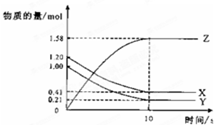
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L·s) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+ Y(g) Z(g) Z(g) |
一定条件下在2 L的密闭容器中充入2 molSO2和2 molO 2,发生反应2SO2(g)+O2(g) 2SO3(g),进行到4 min时,测得n(SO2)="1.2" mol。下列说法正确的是 ( )
2SO3(g),进行到4 min时,测得n(SO2)="1.2" mol。下列说法正确的是 ( )
| A.反应进行到2 min时,容器中n(SO3)可能为0.5 mol |
| B.当v(SO2)∶v(O2)∶v(SO3)=2∶1∶2时该反应达平衡状态 |
| C.温度升高时正反应速率增大,逆反应速率减小 |
| D.4 min内氧气的平均反应速率为0.5 mol·L-1·min-1 |
(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
|
T/℃ |
700 |
800 |
830 |
1 000 |
1 200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应为________反应(填“吸热”“放热”).
(2)能判断该反应是否已达化学平衡状态的依据是________.
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)d.c(CO2)=c(CO)
(3)某温度下,在2 L的密闭容器中,加入1 mol CO2和1 mol H2充分反应达平衡时,CO平衡浓度为0.25 mol/L,试判断此时的温度为________℃.
(4)若在(3)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,H2的物质的量为________.
a.等于1.0 mol b.大于1.0 mol
c.大于0.5 mol d.无法确定
 3C(g),2分钟达到平衡,生成1.5 mol C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol,体积分数为ω2,请回答下列问题,
3C(g),2分钟达到平衡,生成1.5 mol C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol,体积分数为ω2,请回答下列问题,