题目内容
用铂电极电解100mL HNO3与AgNO3的混合液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合液中Ag+的物质的量浓度为( )
| A、1mol/L |
| B、2mol/L |
| C、2.5mol/L |
| D、3mol/L |
考点:电解原理
专题:电化学专题
分析:铂电极为惰性电极,电解HNO3与AgNO3 的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),阴极发生2Ag++2e-=2Ag、2H++2e-=H2↑,阳极发生4OH--4e-=2H2O+O2↑,以此进行计算.
解答:
解:铂电极为惰性电极,电解HNO3与AgNO3 的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),
n(气体)=
=0.1mol,由阳极发生4OH--4e-=2H2O+O2↑可知,生成0.1molO2转移0.4mol电子,
根据电子守恒可知,阴极转移0.4mol电子,则
2H++2e-=H2↑
0.2mol 0.1mol
2Ag++2e-=2Ag
0.2mol 0.2mol
即n(Ag+)=0.2mol,
则原混合溶液中Ag+的物质的量浓度为
=2mol/L,
故选B.
n(气体)=
| 2.24L |
| 22.4L/mol |
根据电子守恒可知,阴极转移0.4mol电子,则
2H++2e-=H2↑
0.2mol 0.1mol
2Ag++2e-=2Ag
0.2mol 0.2mol
即n(Ag+)=0.2mol,
则原混合溶液中Ag+的物质的量浓度为
| 0.2mol |
| 0.1L |
故选B.
点评:本题考查电解原理及氧化还原反应的计算,明确发生的电极反应及电子守恒是解答本题的关键,注意阴极银离子先放电为解答的易错点,题目难度中等.

练习册系列答案
相关题目
下列是某学生自己总结的一些规律,其中正确的是( )
| A、有的无机化学反应不属于化合、分解、置换、复分解中的任何一种反应 |
| B、某物质在固态时能导电,可确认该物质是金属单质 |
| C、一种元素在同一物质中可显示不同价态,但一定是该元素的相邻价态 |
| D、氧化物只可能是氧化产物,不可能是还原产物 |
能大量共存且溶液为无色透明的离子组是( )
| A、Ag+,K+,NO3-,Cl- |
| B、Na+,H+,NO3-,SO42- |
| C、K+,Ca2+,NO3-,CO32- |
| D、Cu2+,Ba2+,Cl-,SO42- |
在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是( )
| A、CO2和SO2中物质的量比为1:1 |
| B、CO2和SO2的密度比为1:1 |
| C、CO2和SO2的物质的量浓度比为11:16 |
| D、CO2和SO2中所含氧原子个数比为16:11 |
下列关于有机化合物的说法正确的组合是( )
①乙醛可发生银镜反应,说明其还原性较强
②乙烯可以与氢气发生加成反应,苯不能与氢气加成
③甲烷和乙烯都可以与氯气反应
④高锰酸钾可以氧化苯和甲苯
⑤用于奥运“祥云”火炬的丙烷是一种清洁燃料
⑥等物质的量的氯气与乙烷在光照条件下反应能制得纯净的一氯乙烷
⑦芳香烃又叫苯的同系物.
①乙醛可发生银镜反应,说明其还原性较强
②乙烯可以与氢气发生加成反应,苯不能与氢气加成
③甲烷和乙烯都可以与氯气反应
④高锰酸钾可以氧化苯和甲苯
⑤用于奥运“祥云”火炬的丙烷是一种清洁燃料
⑥等物质的量的氯气与乙烷在光照条件下反应能制得纯净的一氯乙烷
⑦芳香烃又叫苯的同系物.
| A、①⑤⑥ | B、①③⑤ |
| C、②④⑦ | D、①③⑦ |
下列说法正确的是( )
| A、两种难溶物中溶解度小的物质其KSP不一定小 |
| B、同种酸形成的酸式盐溶解度一定比正盐的溶解度大 |
| C、因为Ksp(BaSO4)=1.08×l0-10,Ksp(BaCO3)=8.1×10-9,所以BaSO4沉淀不可能转化为BaCO3沉淀 |
| D、相同温度下,将足量AgCl固体分别加入同体积的①0.1mo1?L-1盐酸、②0.1mo1?L-1氯化镁溶液、③0.1mo1?L-1硝酸银溶液中,c(Ag+):③>②>① |

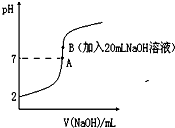 氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF?H++F-.25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示.
氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF?H++F-.25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示.