题目内容
【题目】《天工开物》载:黄矾所出又奇甚,乃即炼皂矾炉侧土墙,刮取下来。染家用之,金色淡者涂炙,立成紫赤也。(皂矾FeSO4·7H2O;黄矾Fe2(SO4)3·10H2O;赤矾Fe2O3)下列有关说法正确的是
A. 皂矾可用于碱性花木土壤补铁
B. 皂矾变为黄矾是受热脱水过程
C. 黄矾受热分解可以获得赤矾
D. 矾是含结晶水的硫酸盐矿石
【答案】C
【解析】FeSO4溶液呈酸性,不能用于碱性花木土壤补铁,故A错误;FeSO4·7H2O变为Fe2(SO4)3·10H2O是氧化过程,故B错误;Fe2(SO4)3·10H2O受热分解可以生成Fe2O3、SO3、H2O,故C正确;赤矾Fe2O3 不是硫酸盐,故D错误。

【题目】氮和硫的化合物在科研、生活及化学工业中具有重要的应用。
(1)已知:SO2(g)+1/2O2(g)=SO3(g) H=-99kJ·mol-1
SO2(g)+NO2(g)=SO3(g)+ NO(g) H=-41.8kJ·mol-1
CO(g)+1/2O2(g)=CO2(g) H=-283kJ·mol-1
请写出CO和NO2反应生成CO2和NO的热化学反应方程式_________________,1molCO和1molNO2反应生成CO2和NO的能量反应示意图中的E2=_______kJ·mol-1

(2)可通过反应2CO(g)+SO2(g)![]() 2CO2(g)+S(l)来消除锅炉烟道气中的有毒气体,某温度下向密闭容器中通入一定量的SO2和CO气体发生反应,5分钟后达平衡,生成0.5 mol/L的CO2。
2CO2(g)+S(l)来消除锅炉烟道气中的有毒气体,某温度下向密闭容器中通入一定量的SO2和CO气体发生反应,5分钟后达平衡,生成0.5 mol/L的CO2。
①反应开始至平衡时,SO2的平均反应速率v(SO2)=________;
②其他条件不变时,SO2的平衡转化率随反应温度变化如图,请用简洁文字解释原因_________________________________________;

(3)25℃,在0.10 molL1H2S溶液中,溶液pH与c(S2)关系如下表(忽略溶液体积的变化、H2S的挥发),某溶液含0.020 molL1Mn2+、0.1 molL1H2S,当溶液的pH=5时,
Mn2+开始沉淀,则MnS的溶度积Ksp =________________;
pH | 3 | 5 | 7 | 9 | 11 |
c(S2-)/ molL1 | 1.4×1015 | 1.4×1011 | 6.8×108 | 1.3×105 | 1.3×103 |
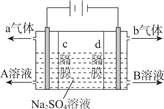
(4)一种脱除废水中NH4+ 的电化学装置如图所示,请写出阳极的电极反应方程式:____________, 电解一段时间后阴极周围溶液的pH_____(填“增大”, “减小”或“不变”)。