题目内容
(I )实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:Al
| H2SO4 |
| NaOH |
方案2:Al
| NaOH |
| AlO | - 2 |
| H2SO4 |
方案3:
|
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案
(II)工业上冶炼铝的流程图如图所示:

在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe203质量分数的数据如下:
| Al2O3 | Fe2O3 | 其他杂质 | |
| 铝土矿 | 55% | 16% | - |
| 赤泥 | 15% | 48% | 一 |
(2)电解氧化铝生产铝时,阳极的电极反应式为
(3)假设其它杂质不参加反应,则每生产3.4t纯净的氧化铝,需铝土矿
(Ⅱ)(1)向偏铝酸钠中通入二氧化碳反应会生成氢氧化铝沉淀,碳酸钠可以和氢氧化钙发生复分解反应;
(2)电解池中,阳极是惰性电极时,该极上是阴离子发生失电子的氧化反应;
(3)根据铝元素守恒来计算回答.
Al~OH-~[Al(OH)4]-,Al3++3[Al(OH)4]-=4Al(OH)3↓,所以制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案3,故答案为:3;
(Ⅱ)(1)向偏铝酸钠中通入二氧化碳反应会生成氢氧化铝沉淀,即2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓,碳酸钠可以和氢氧化钙发生复分解反应Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,
故答案为:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)电解池中,阳极是惰性电极时,该极上是阴离子O2-发生失电子的氧化反应:2O2--4e-=O2↑,
故答案为:2O2--4e-=O2↑;
(3)根据铝土矿中氧化铝的质量分数为55%,所以每生产3.4t纯净的氧化铝,需铝土矿的质量:
| 3.4 |
| 55% |
故答案为:6.18.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案
| |||||||||||||||||||||||
铝是国民经济发展的重要材料,铝在地壳中的含量约占8% ,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(I )实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:
方案3 : o
o
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案_____________________。
(II)工业上冶炼铝的流程图如图16所示:

在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe203质量分数的数据如下:
|
|
Al2O3 |
Fe2O3 |
其他杂质 |
|
铝土矿 |
55% |
16% |
— |
|
赤泥 |
15% |
48% |
一 |
(1) 书写化学方程式,反应①_________,反应②________________
(2) 电解氧化铝生产铝时,阳极的电极反应式为________________。
(3) 假设其它杂质不参加反应,则每生产3.4t纯净的氧化铝,需铝土矿________t
铝是国民经济发展的重要材料,铝在地壳中的含量约占8%,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(I )实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:
方案3 :
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案_____________________。
(II)工业上冶炼铝的流程图如图所示:
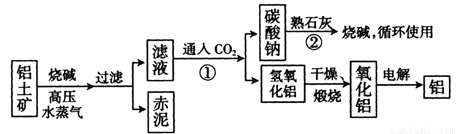
在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe203质量分数的数据如下:
|
|
Al2O3 |
Fe2O3 |
其他杂质 |
|
铝土矿 |
55% |
16% |
— |
|
赤泥 |
15% |
48% |
一 |
(1) 书写化学方程式,反应①_______ ,
反应②______________ __
(2) 电解氧化铝生产铝时,阳极的电极反应式为____________ _。
(3) 假设其它杂质不参加反应,则每生产3.4t纯净的氧化铝,需铝土矿______ __t


