题目内容
【题目】在恒温(500K)、体积为2.0L的密闭容器中通入1.0molN2和1molH2发生合成氨反应,20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的总物质的量为1.6mol。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=______。
(2)该反应的热化学方程式为______。
(3)若拆开1molH—H键和1molN![]() N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______kJ。
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______kJ。
【答案】0.01molL-1min-1 N2(g)+3H2(g)2NH3(g) △H=92.4kJ/mol 391
【解析】
在恒温,体积为2L的密闭容器中通入1molN2和1molH2,20min后达到平衡,测得反应放出的热量为 18.4 kJ,混合气体的物质的量为1.6mol;设消耗的氮气为n mol,则:
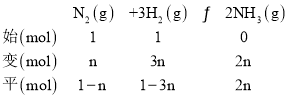
所以:1-n+1-3n+2n=1.6,解得n=0.2,1mol氮气反应放出的热量为18.4kJ×![]() =92kJ,
=92kJ,
(1)根据化学反应速率v=![]() 计算;
计算;
(2)1mol氮气反应放出的热量为18.4kJ×5=92kJ,据此书写热化学方程式;
(3)根据反应热△H=反应物的键能和-生成物的键能和计算解答。
在恒温,体积为2L的密闭容器中通入1molN2和1molH2,20min后达到平衡,测得反应放出的热量为 18.4 kJ,混合气体的物质的量为1.6mol;设消耗的氮气为n mol,则:
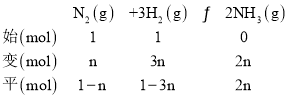
所以:1-n+1-3n+2n=1.6,解得n=0.2,1mol氮气反应放出的热量为18.4kJ×![]() =92kJ,
=92kJ,
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=![]() =
= = 0.01molL-1min-1;
= 0.01molL-1min-1;
(2)1mol氮气反应放出的热量为18.4kJ×5=92kJ,则发生反应的热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=-92kJ/mol;
(3)设拆开1 mol N—H键需要的能量是QkJ,则反应热△H=反应物的键能和-生成物的键能和=(946kJ/mol)+(436 kJ/mol)×3-(Q kJ/mol)×6=-92kJ/mol,解得:Q=391kJ。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案