题目内容
有一瓶14%的氢氧化钾溶液,加热蒸发掉100g水后,得到28%的氢氧化钾溶液80mL,所得溶液的浓度为
- A.5mol/L
- B.6mol/L
- C.6.25mol/L
- D.6.5mol/L
C
分析:根据蒸发前后溶质的质量不变,计算出溶液的质量,根据质量分数计算溶质的物质的量,进而计算溶液的物质的量浓度.
解答:设14%氢氧化钾溶液的质量为x,蒸发前后溶质的质量不变,则有x×14%=(x-100g)×28%,x=200g,
28%的氢氧化钾溶液中含有氢氧化钾的物质的量为 =0.5mol,
=0.5mol,
所得溶液的物质的量浓度为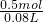 =6.25mol/L,
=6.25mol/L,
故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,本题注意计算蒸发后溶液的质量为解答该题的关键.
分析:根据蒸发前后溶质的质量不变,计算出溶液的质量,根据质量分数计算溶质的物质的量,进而计算溶液的物质的量浓度.
解答:设14%氢氧化钾溶液的质量为x,蒸发前后溶质的质量不变,则有x×14%=(x-100g)×28%,x=200g,
28%的氢氧化钾溶液中含有氢氧化钾的物质的量为
 =0.5mol,
=0.5mol,所得溶液的物质的量浓度为
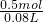 =6.25mol/L,
=6.25mol/L,故选C.
点评:本题考查物质的量浓度的计算,题目难度不大,本题注意计算蒸发后溶液的质量为解答该题的关键.

练习册系列答案
相关题目