题目内容
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO42-的物质的量浓度为
- A.0.4 mol·L-1
- B.0.1 mol·L-1
- C.0.2 mol·L-1
- D.0.3 mol·L-1
B
试题分析:溶液中Al3+为1.62g,物质的量为1.62g÷27g/mol=0.06mol,根据电荷守恒可知,溶液中n(SO42-)=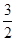 ×n(Al3+)=0.09mol。加入的氢氧化钡的物质的量为0.1mol/L×0.3=0.03mol,根据方程式SO42-+Ba2+=BaSO4↓可知SO42-剩余,剩余SO42-的物质的量为0.09mol-0.03mol=0.06mol,所以反应后溶液中SO42-的物质的量的浓度为0.06mol÷(0.3L+0.3L)=0.1mol/L,答案选B。
×n(Al3+)=0.09mol。加入的氢氧化钡的物质的量为0.1mol/L×0.3=0.03mol,根据方程式SO42-+Ba2+=BaSO4↓可知SO42-剩余,剩余SO42-的物质的量为0.09mol-0.03mol=0.06mol,所以反应后溶液中SO42-的物质的量的浓度为0.06mol÷(0.3L+0.3L)=0.1mol/L,答案选B。
考点:考查离子反应、物质的量浓度计算
试题分析:溶液中Al3+为1.62g,物质的量为1.62g÷27g/mol=0.06mol,根据电荷守恒可知,溶液中n(SO42-)=
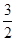 ×n(Al3+)=0.09mol。加入的氢氧化钡的物质的量为0.1mol/L×0.3=0.03mol,根据方程式SO42-+Ba2+=BaSO4↓可知SO42-剩余,剩余SO42-的物质的量为0.09mol-0.03mol=0.06mol,所以反应后溶液中SO42-的物质的量的浓度为0.06mol÷(0.3L+0.3L)=0.1mol/L,答案选B。
×n(Al3+)=0.09mol。加入的氢氧化钡的物质的量为0.1mol/L×0.3=0.03mol,根据方程式SO42-+Ba2+=BaSO4↓可知SO42-剩余,剩余SO42-的物质的量为0.09mol-0.03mol=0.06mol,所以反应后溶液中SO42-的物质的量的浓度为0.06mol÷(0.3L+0.3L)=0.1mol/L,答案选B。考点:考查离子反应、物质的量浓度计算

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol/L Ba(OH)2溶液300 mL,反应后溶液中SO的物质的量浓度为( )
| A.0.4 mol/L | B.0.3 mol/L | C.0.2 mol/L | D.0.1 mol/L |
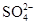 的物质的量浓度为(忽略溶液体积的变化)
( )
的物质的量浓度为(忽略溶液体积的变化)
( )