题目内容
【题目】一定条件下,在水溶液中1molCl、ClO x (x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
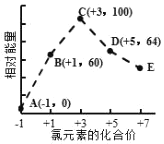
A.这些离子中结合H+能力最强的是E
B.A、B、C、D、E五种微粒中C最稳定
C.C→B+D的反应,反应物的总键能小于生成物的总键能
D.B→A+D是吸热反应
【答案】C
【解析】
A.对应酸的酸性越弱,则酸根离子结合氢离子的能力越强,高氯酸的酸性最强,因此ClO4 结合H+能力最弱,故A错误;
B.能量越低越稳定,则A、B、C、D、E五种微粒中A最稳定,C最不稳定,故B错误;
C.C→B+D为2ClO2-=ClO3-+ClO-,反应热△H =生成物的总能量-反应物的总能量=(64kJ/mol+60kJ/mol)-2×100kJ/mol=-76kJ/mol,则反应物的总键能小于生成物的总键能,故C正确;
D.B→A+D为3ClO-=ClO3-+2Cl-,反应热△H =(64kJ/mol+2×0kJ/mol)-3×60kJ/mol=-116kJ/mol,为放热反应,故D错误;
故选C。

练习册系列答案
相关题目
【题目】下列有关实验的操作正确的是
实验目的 | 实验操作 | |
A | 配制浓度为0.010 | 用托盘天平称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
B | 浓盐酸与MnO2反应制备纯净Cl2 | 气体产物先通过浓硫酸,后通过饱和食盐水 |
C | 配制稀硫酸 | 先将浓硫酸加入烧杯中,后倒入蒸馏水 |
D | 排水法收集KMnO4分解产生的O2 | 先移出导管,后熄灭酒精灯 |
A.AB.BC.CD.D