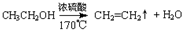题目内容
 |
 |
 |
 |
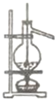
| 钾与水的反应 A |
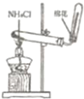
实验室制取氨气 B |
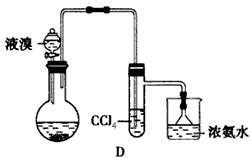
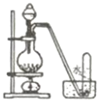
石油分馏 C |
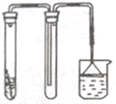
闻气体的方法 D |
 |
 |
 |
 |
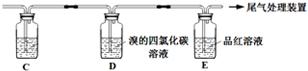
| 二氧化锰与浓盐酸反应制取氯气 E |
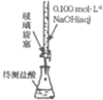
用标准液滴定待测液 F |
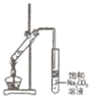
制取NO2气体 G |
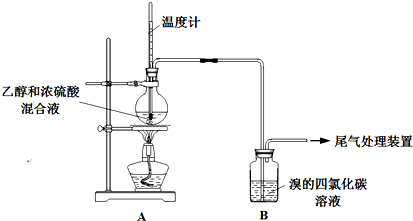
合成乙酸乙酯 H |
B、氯化铵分解为氨气和氯化氢,二者遇冷立即化合再生成氯化铵,这样不能收集到氨气,故B错误;
C、分馏装置温度计控制的是沸腾出来的蒸气的温度,u影放在支管口处位置,故C错误;
D、应该用扇气味闻气法来闻气体的气味,故D正确;
E、氨气极易溶于水,可以用排空气法收集,不能排水法收集,故E错误;
F、氢氧化钠标准液要放在碱式滴定管中,不能用酸式滴定管,故F错误;
G、可以用金属铜和浓硝酸反应来制取二氧化氮气体,用向上排空气法收集,尾气要用氢氧化钠进行尾气处理,故G正确;
H、用乙酸和乙醇来合成乙酸乙酯,并用饱和的碳酸钠溶液来吸收,故H正确.
故选B、C、E、F.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
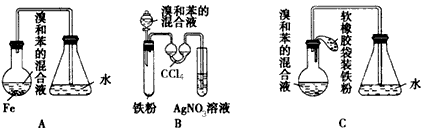
小学生10分钟应用题系列答案)单晶硅是信息产业中重要的基础材料。工业上可用焦炭与二氧化硅的混合物在高温下与氯气反应生成SiCl4和CO,SiCl4经提纯后用氢气还原得高纯硅。以下是实验室制备SiCl4的装置示意图。
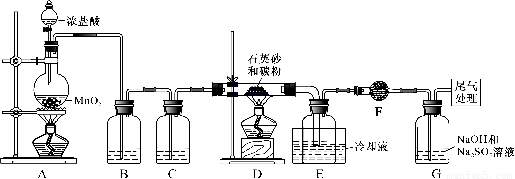
实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4、AlCl3、FeCl3遇水均易水解,有关物质的物理常数见下表:
物质 | SiCl4 | AlCl3 | FeCl3 |
沸点/℃ | 57.7 | - | 315 |
熔点/℃ | -70.0 | - | - |
升华温度/℃ | - | 180 | 300 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:_____________, 装置D的硬质玻璃管中发生反应的化学方程式是????????????????????????? 。
(2)装置C中的试剂是?????????? ; D、E间导管短且粗的原因是????????????? 。
(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-;假设3:?????? 。
【设计方案,进行实验】可供选择的实验试剂有:3 mol/L H2SO4、1 mol/L NaOH、0.01 mol/L KMnO4、溴水、淀粉-KI、品红等溶液。
取少量吸收液于试管中,滴加3 mol/L H2SO4至溶液呈酸性,然后将所得溶液分置于a、b、c三支试管中,分别进行下列实验。请完成下表:
序号 | 操? 作 | 可能出现的现象 | 结论 |
① | 向a试管中滴加几滴????????? 溶液 | 若溶液褪色 | 则假设1成立 |
若溶液不褪色 | 则假设2或3成立 | ||
② | 向b试管中滴加几滴????????? 溶液 | 若溶液褪色 | 则假设1或3成立 |
若溶液不褪色 | 假设2成立 | ||
③ | 向c试管中滴加几滴????????? 溶液 |
| 假设3成立 |
单晶硅是信息产业中重要的基础材料。工业上可用焦炭与二氧化硅的混合物在高温下与氯气反应生成SiCl4和CO,SiCl4经提纯后用氢气还原得高纯硅。以下是实验室制备SiCl4的装置示意图。
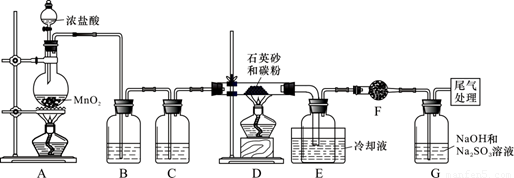
实验过程中,石英砂中的铁、铝等杂质也能转化为相应氯化物,SiCl4、AlCl3、FeCl3遇水均易水解 ,有关物质的物理常数见下表:
,有关物质的物理常数见下表:
|
物质 |
SiCl4 |
AlCl3 |
FeCl3 |
|
沸点/℃ |
57.7 |
- |
315 |
|
熔点/℃ |
-70.0 |
- |
- |
|
升华温度/℃ |
- |
180 |
300 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式:_____________, 装置D的硬质玻璃管中发生反应的化学方程式是 。
 (2)装置C中的试剂是
; D、E间导管短且粗的原因是
。
(2)装置C中的试剂是
; D、E间导管短且粗的原因是
。
 (3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
(3)G中吸收尾气一段时间后,吸收液中肯定存在OH-、Cl-和SO42-。请设计实验,探究该吸收液中可能存在的其他酸根离子(忽略空气中CO2的影响)。
【提出假设】假设1:只有SO32-;假设2:既无SO32-也无ClO-;假设3: 。
【设计方案,进行实验】可供选择的实验试剂有:3 mol/L H2SO4、1 mol/L NaOH、0.01 mol/L KMnO4、溴水、淀粉-KI、品红等溶液。
取少量吸收液于试管中,滴加3 mol/L H2SO4至溶液呈酸性,然后将所得溶液分置于a、b、c三支试管中,分别进行下列实验。请完成下表:
|
序号 |
操 作 |
可能出现的现象 |
结论 |
|
① |
向a试管中滴加几滴 溶液 |
若溶液褪色 |
则假设1成立 |
|
若溶液不褪色 |
则假设2或3成立 |
||
|
② |
向b试管中滴加几滴 溶液 |
若溶液褪色 |
则假设1或3成立 |
|
若溶液不褪色 |
假设2成立 |
||
|
③ |
向c试管中滴加几滴 溶液 |
|
假设3成立 |