题目内容
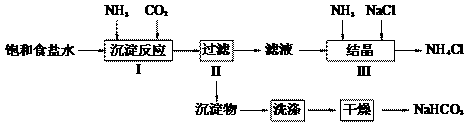
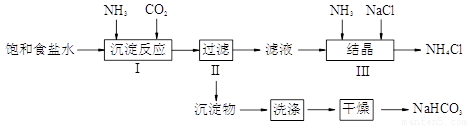
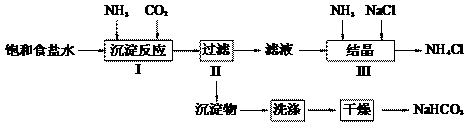
实验室欲制取少量NaHCO3与NH4Cl.实验步骤如下:
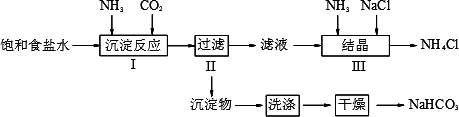
请回答:
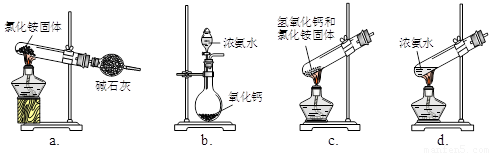
(1)步骤Ⅰ、Ⅲ中需用到氨气,下列装置可用于实验室制氨气的是________.(填序号)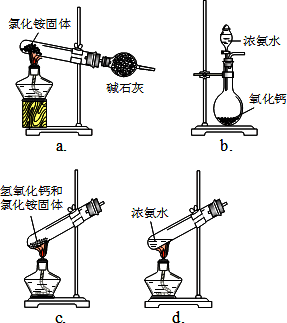
(2)写出步骤I中发生的化学反应方程式________.若用下图装置进行该沉淀反应.实验时,须先从________(填“a”、“b”或“c”)管通入________气体.
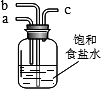
(3)步骤Ⅲ向滤液中通入氨气,加入细小食盐颗粒,可使NH4Cl晶体单独结晶析出.
①此处通入氨气的作用是________.
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
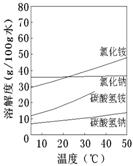
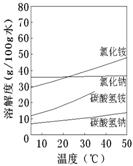
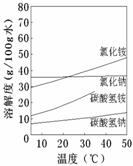
②已知四种相关物质不同温度下的溶解度曲线如图所示.
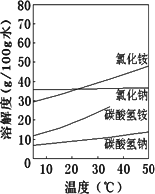
结晶时宜采用________(填“蒸发结晶”或“降温结晶”).
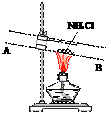
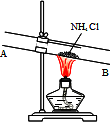
③有人设计了如下图所示的装置来验证所得的晶体中含有NH4+.具体操作:取少量晶体于硬质试管,对晶体部位加热.并在________(填“A”或“B”)处放置________试纸,观察现象.
(4)请按提示完成NaHCO3含量分析的实验设计.
试剂:盐酸、澄清石灰水、氢氧化钡溶液、蒸馏水;
仪器:电子天平、烧杯、漏斗、玻璃棒、干燥器等
①________溶于水,加入________.
②过滤、洗涤、烘干,冷却、称量,并进行________操作(写操作名称).
③计算.若数据处理时将所得固体质量1.977 g错看为1.971 g,由此产生的相对误差为________.
解析:
|
(1)b、d(2分) (2)NaCl+NH3+CO2+H2O→NaHCO3↓+NH4Cl;a、NH3(共1分) (3)①a、c(共1分);②降温结晶;③A、湿润红色石蕊试纸(共1分) (4)①准确称量样品,加入足量Ba(OH)2溶液;②恒重;③-0.3%(2分) |

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案实验室欲制取少量NaHCO3与NH4Cl。实验步骤如下:

请回答:
(1)步骤I、III中需用到氨气,下列装置可用于实验室制氨气的是_________。(填序号)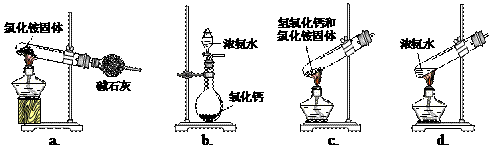
| (2)写出步骤I中发生的化学反应方程式 _______________________________________________________。 若用右图装置进行该沉淀反应。实验时,须先从_____(填“a”、“b”或“c”)管通入_____气体。 |
|
(3)步骤III向滤液中通入氨气,加入细小食盐颗粒,可使NH4Cl晶体单独结晶析出。
 ①此处通入氨气的作用是_________。
①此处通入氨气的作用是_________。
a. 增大NH4+的浓度,使NH4Cl更多地析出
b. 使NaHCO3更多地析出
c. 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
②已知四种相关物质不同温度下的溶解度曲线如图所示。
结晶时宜采用___________(填“蒸发结晶”或“降温结晶”)。
③有人设计了如下图所示的装置来验证所得的晶体中含有NH4+。
 具体操作:取少量晶体于硬质试管,对晶体部位加热。并在_____
具体操作:取少量晶体于硬质试管,对晶体部位加热。并在_____
(填“A”或“B”)处放置______________试纸,观察现象。
(4)请按提示完成NaHCO3含量分析的实验设计。
试剂:盐酸、澄清石灰水、氢氧化钡溶液、蒸馏水;
仪器:电子天平、烧杯、漏斗、玻璃棒、干燥器等
① _________________溶于水,加入__________________________。
②过滤、洗涤、烘干,冷却、称量,并进行_____________操作(写操作名称)。
③计算。若数据处理时将所得固体质量1.977 g错看为1.971 g,由此产生的相对误差为_____。
实验室欲制取少量NaHCO3与NH4Cl。实验步骤如下:
请回答:
(1)步骤I、III中需用到氨气,下列装置可用于实验室制氨气的是_________。(填序号)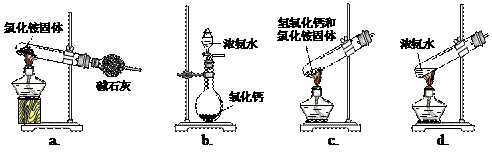
|
(2)写出步骤I中发生的化学反应方程式 _______________________________________________________。 若用右图装置进行该沉淀反应。实验时,须先从_____(填“a”、“b”或“c”)管通入_____气体。 |
|
(3)步骤III向滤液中通入氨气,加入细小食盐颗粒,可使NH4Cl晶体单独结晶析出。
 ①此处通入氨气的作用是_________。
①此处通入氨气的作用是_________。
a. 增大NH4+的浓度,使NH4Cl更多地析出
b. 使NaHCO3更多地析出
c. 使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
②已知四种相关物质不同温度下的溶解度曲线如图所示。
结晶时宜采用___________(填“蒸发结晶”或“降温结晶”)。
③有人设计了如下图所示的装置来验证所得的晶体中含有NH4+。
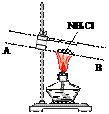 具体操作:取少量晶体于硬质试管,对晶体部位加热。并在_____
具体操作:取少量晶体于硬质试管,对晶体部位加热。并在_____
(填“A”或“B”)处放置______________试纸,观察现象。
(4)请按提示完成NaHCO3含量分析的实验设计。
试剂:盐酸、澄清石灰水、氢氧化钡溶液、蒸馏水;
仪器:电子天平、烧杯、漏斗、玻璃棒、干燥器等
① _________________溶于水,加入__________________________。
②过滤、洗涤、烘干,冷却、称量,并进行_____________操作(写操作名称)。
③计算。若数据处理时将所得固体质量1.977 g错看为1.971 g,由此产生的相对误差为_____。