题目内容
某化学反应反应物的总能量大于生成物的总能量,则该反应( )
| A.是吸热反应 | B.是放热反应 |
| C.不一定遵循质量守恒定律 | D.不需要加热就一定能发生 |
B
解析试题分析:某化学反应反应物的总能量大于生成物的总能量,则该反应是放热反应,无论是放热反应还是吸热反应都要在一定的条件下才能发生,在发生反应时,一定会遵循质量守恒定律。故选项是B。
考点:考查化学反应的分类及反应符合的规律及条件的关系的知识。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片和稀硫酸反应 | B. 与 与 反应 反应 |
C.灼热的炭与 反应 反应 | D.甲烷在 中燃烧 中燃烧 |
如图所示,把下列物质分别加入装有水的锥形瓶里,立即塞紧带有U形管的塞子,已知U形管内预先装有少量水(为方便观察,预先将水染成红色),结果U形管左边液面升高,则加入的物质可能是( ) 
| A.NaOH固体 | B.浓硫酸 | C.NH4NO3晶体 | D.Na2O2固体 |
下列有关热化学方程式的叙述正确的是
| A.2H2(g)+O2(g)===2H2O(g);△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ |
| B.已知C(石墨,s)="==" C(金刚石,s) △H>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l);△H=-57.4 kJ/mol |
| D.已知2C(s)+2O2(g)==2CO2(g);△H1 ;2C(s)+O2(g)="2CO(g)" △H2。则△H1>△H2 |
已知298 K时,合成氨反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
2NH3(g) ΔH=-92.0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量为(假定测量过程中没有能量损失) ( )
| A.一定小于92.0 kJ | B.一定大于92.0 kJ |
| C.一定等于92.0 kJ | D.无法确定 |
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如下图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
下列说法正确的是( )
| A.1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ |
| B.1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
 键
键
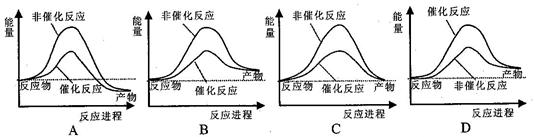
 2 CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1的反应来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是
2 CO2 (g) +S (g) ΔH= +8.0 kJ·mol-1的反应来减少污染,使用新型催化剂加快反应。下列有关该反应过程的能量变化示意图正确的是