题目内容
11.下列化学用语表达正确的是( )| A. | N2的电子式: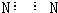 | B. | S2-的结构示意图: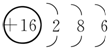 | ||
| C. | 次氯酸的结构式:H-O-Cl | D. | ${\;}_{40}^{65}$Zr和${\;}_{40}^{67}$Zr是同种核素 |
分析 A.氮气分子中,N原子最外层达到8电子稳定结构,漏掉了氮原子的1对孤电子对;
B.硫离子的核外电子总数为18,最外层为8个电子;
C.次氯酸的中心原子为O原子,分子中存在1个氧氢键和1个氧氯键;
D.同种核素具有相同的质子数和中子数.
解答 解:A.氮气中含有氮氮三键,氮气正确的电子式为: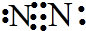 ,故A错误;
,故A错误;
B.硫离子的核外电子总数为18,其离子结构示意图为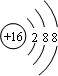 ,故B错误;
,故B错误;
C.次氯酸中存在1个氢氧键和1个氧氯键,次氯酸的结构式为:H-O-Cl,故C正确;
D.二者的质子数相同、中子数不同,二者互为同位素,不是同一种核素,故D错误;
故选C.
点评 本题考查了常见化学用语的书写判断,题目难度中等,注意掌握原子结构示意图与离子结构示意图、电子式、核素、结构式等化学用语的概念及书写原则,试题培养了学生的规范答题能力.

练习册系列答案
相关题目
1.用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅的反应如下:3SiCl4(g)+2N2(g)+6H2(g)$\frac{\underline{\;高温\;}}{\;}$Si3N4(s)+12HCl(g)△H<0,一定温度下,恒容密闭容器中进行该反应,下列措施能增大正反应的反应速率的是( )
| A. | 分离出少量氮化硅 | B. | 降低温度 | ||
| C. | 充入氮气 | D. | 充入氦 |
19.分子式为C3H8O的醇与C4H8O2的羧酸浓H2SO4存在时共热生成的酯有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
6.下列含有非极性键的化合物是( )
| A. | MgCl2 | B. | Na2O2 | C. | H2O | D. | CH4 |
20.苹果酸的结构简式为 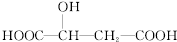 ,下列说法正确的是( )
,下列说法正确的是( )
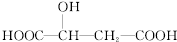 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 1mol苹果酸可与3 mol NaOH发生中和反应 | |
| B. | 1mol苹果酸与足量金属Na反应生成1mol H2 | |
| C. | 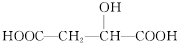 与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | 苹果酸中能发生酯化反应的官能团有2种 |
1.有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、
HCO3-,取该溶液进行如下实验,下列说法中正确的是( )
HCO3-,取该溶液进行如下实验,下列说法中正确的是( )
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加几滴石蕊溶液 | 溶液变红色 |
| ②取少量该溶液,加入铜片和浓硫酸,加热 | 有无色气体产生,遇空气可以变成红棕色 |
| ③取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| ⑤取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
| A. | 溶液中一定存在的离子是SO42-、Mg2+、Al3+、Cl- | |
| B. | 溶液中一定存在的离子是NO3-、SO42-、Mg2+、Al3+ | |
| C. | 溶液中肯定不存在的离子是Fe2+、HCO3-、I-、SO42- | |
| D. | 溶液中肯定不存在的离子是Fe2+、HCO3-、Mg2+、I-、Ba2+ |
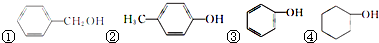 (填序号)
(填序号)
 ; Z在周期表中的位置是第三周期ⅥA族;B元素的名称为碳.
; Z在周期表中的位置是第三周期ⅥA族;B元素的名称为碳.