题目内容
【题目】某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验。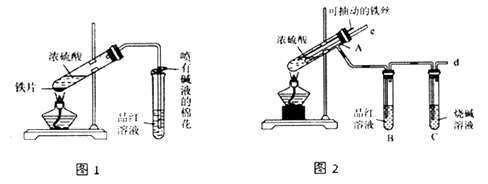
(1)比较两实验装置,图2装置的优点是:
①能更好地吸收有毒气体SO2 , 防止其污染环境;②。
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻值SO2 气体逸出而防止污染环境;二是。
(3)能说明有SO2气体产生的实验现象是。
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入适量水中为试样,试样中所含金属离子的成分有 以下三种可能:
I:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A 稀HCl溶液 B 稀硫酸 C KSCN溶液 D KMnO4溶液
E NaOH溶液 F 淀粉KI溶液 G H2O2溶液
验证Ⅱ:取试样,先滴加少量的(填试剂序号,下同),振荡,再滴加少量的 , 根据溶液颜色的变化可确定假设Ⅱ是否正确。
验证Ⅲ:步骤1.取试样,滴加少量的(填试剂序号,溶液的颜色变色,则试样中含有Fe3+ , 发生反应的离子方程式为;
步骤2.再取适量的试样,滴加少量的(填试剂序号),溶液颜色的变化为 , 则试样中含有Fe2+。
【答案】
(1)便于控制反应的发生和停止
(2)停止加热时,防止倒吸或平衡压强
(3)品红溶液褪色
(4)C;G;C(或F);红(或蓝);Fe3++3SCN-=Fe(SCN)3或2Fe3++2I-=2Fe2+ +I2;D;酸性KMmO4溶液的浅红色褪去
【解析】
(1)比较两实验装置,图2装置的优点是:①用烧碱处理尾气,能更好地吸收有毒气体SO2 , 防止其污染环境;②铁丝能自由抽动,便于控制反应的发生和停止。
(2)导气管e可以插入溶液中,所以导管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到“液封”作用阻值SO2 气体逸出而防止污染环境;停止加热时,装有铁和浓硫酸的试管中压强减小,有这样一根导管能防止倒吸或平衡压强。
(3)二氧化硫的特性是使品红溶液褪色,因此能说明有SO2气体产生的实验现象是品红溶液褪色。
(4)铁离子与硫氰化钾反应可以生成血红色的溶液,用此来检验三价铁离子,二价铁离子的检验是利用其还原性。亚铁离子能被高锰酸钾或双氧水氧化,然后再利用硫氰化钾来进行确定。验证Ⅱ:根据上述分析,取试样,先滴加少量的C(KSCN溶液),振荡,无现象,再滴加少量的G(H2O2 ),若溶液变成血红色,说明只含有Fe2+。
验证Ⅲ:步骤1验证Fe3+是否存在,取试样,滴加少量的KSCN溶液(C)若溶液的颜色变血红色,则试样中含有Fe3+ , 发生反应的离子方程式为Fe3++3SCN-=Fe(SCN)3;
步骤2验证Fe2+是否存在,再取适量的试样,滴加少量的KMnO4 溶液(D),酸性KMnO4溶液的浅红色褪去,则试样中含有Fe2+。
(1)比较两装置图的不同之处,发现有3处要注意:①图2的铁丝是可抽动的,说明可以随时控制反应的发生与停止②图2用氢氧化钠溶液吸收尾气SO2比图1效果好(图1棉花只会蘸取少量碱吸收效果差,而且不密封)③反应装置中多出了一根导管e,处于发生装置和性质实验之连接处,可用于平衡压强,起到液封和防止倒吸的作用。
(2)见上述分析
(3)二氧化硫的漂白性实验常用于检验SO2
(4)检验三价铁离子,利用铁离子与硫氰化钾反应可以生成血红色的溶液的特性反应
通常检验二价铁离子,需结合三价铁离子的特性反应,常先滴加少量的C(KSCN溶液),振荡,无现象(排除Fe3+),再加强氧化剂(氯水、双氧水、酸性高锰酸钾溶液等),若出现血红色,则原溶液中含有Fe2+
若Fe2+、Fe3+同时存在,可取两次试剂做实验,分别检验Fe3+、Fe2+
取试样,滴加少量的KSCN溶液,若溶液的颜色变血红色,则试样中含有Fe3+
再取适量的试样,滴加少量的KMnO4 溶液(选取有颜色的强氧化剂,起到指示剂的作用),酸性KMnO4溶液的浅红色褪去,则试样中含有Fe2+。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)2Z(g),各组分在不同时刻的浓度如下表:下列说法正确的是( )
物质 | X | Y | Z |
初始浓度/molL﹣1 | 0.1 | 0.2 | 0 |
2min末浓度/molL﹣1 | 0.08 | a | b |
平衡浓度/molL﹣1 | 0.05 | 0.05 | 0.1 |
A.平衡时,X的转化率为20%
B.t℃时,该反应的平衡常数为40
C.增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动
D.前2min内,用Y的变化量表示的平均反应速率v(Y)=0.03molL﹣1min﹣1


