题目内容
2.下列实验能达到目的是( )| A. | 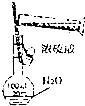 稀释浓硫酸 | B. | 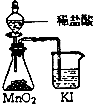 比较MnO2、CI2、I2的氧化性 | ||
| C. | 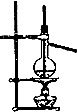 分离乙醇和水 | D. | 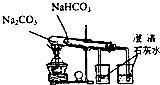 比较Na2CO3、NaHCO3的热稳定性 |
分析 A.容量瓶不能稀释溶液;
B.稀盐酸和二氧化锰不反应;
C.温度计测量蒸汽的温度;
D.碳酸钠稳定,碳酸氢钠加热分解.
解答 解:A.容量瓶不能稀释溶液,稀释溶液应用烧杯,故A错误;
B.稀盐酸和二氧化锰不反应,应用浓盐酸加热,故B错误;
C.温度计测量蒸汽的温度,应与蒸馏烧瓶支管口相平,故C错误;
D.碳酸钠稳定,碳酸氢钠加热分解,小试管中应为碳酸氢钠,能起对比作用,故D正确.
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及性质实验及实验基本操作等,把实验基本操作和反应原理为解答的关键,注意实验装置的作用及实验的评价性分析,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
12.电子表中电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,放电时锌极上的电极反应是:Zn+2OH-2e-═Zn(OH)2;氧化银电极上的反应式为:Ag2O+H2O+2e-═2Ag+2OH-,总反应式为:Ag2O+H2O+Zn═Zn(OH)2+2Ag.下列说法正确的是( )
| A. | 锌是负极,氧化银是正极 | |
| B. | 锌发生还原反应,氧化银发生氧化反应 | |
| C. | 溶液中OH-向正极移动,K+、H+向负极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液的pH逐渐增大 |
17.下列各组物质性质的比较中,有一组的递变规律与其他不同的是( )
| A. | 还原性Cl-、Br-、I- | B. | 碱性:Na0H、Mg(OH)2、Al(OH)3 | ||
| C. | 稳定性HCl、H2S、PH3 | D. | 酸性:HC1O4、H2SO4、H2CO3 |
 ;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)
;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka=4×10?12(提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解) .
. .
.