题目内容
t℃时在VL密闭容器中通入a g SO3(g),此时容器内的压强为P,当反应2SO3(g)?2SO2(g)+O2(g)达到平衡状态时恢复至原温度,压强变为1.25P,则平衡混合气体的平均相对分子质量为( )
分析:在相同温度、相同体积下,气体的物质的量之比等于压强之比,根据压强变化计算反应后气体的物质的量,可计算出平衡混合气体的平均相对分子质量.
解答:解:n(SO3)=
mol,设平衡时气体的物质的量为n,
在相同温度、相同体积下,气体的物质的量之比等于压强之比,
则
=1.25,
n=
mol,
反应前后气体的质量不变,
则则平衡混合气体的平均相对分子质量为=
=64,
故选B.
| a |
| 80 |
在相同温度、相同体积下,气体的物质的量之比等于压强之比,
则
| n | ||
|
n=
| a |
| 64 |
反应前后气体的质量不变,
则则平衡混合气体的平均相对分子质量为=
| a | ||
|
故选B.
点评:本题考查化学平衡的计算,题目难度中等,本题侧重于混合气体平均相对分子质量的计算,解答本题的关键是根据压强关系计算物质的量.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
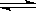 2SO2(g)+O2(g)达到平衡状态时恢复至原温度,压强变为1.25P ,则平衡混合气体的平均相对分子质量为
2SO2(g)+O2(g)达到平衡状态时恢复至原温度,压强变为1.25P ,则平衡混合气体的平均相对分子质量为