题目内容
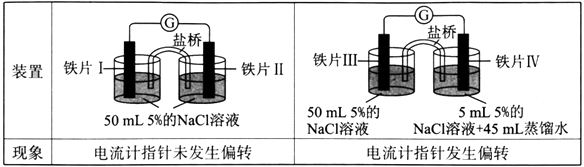
【题目】将两根铁钉分别缠绕铜丝和铝条,放人滴有混合溶液的容器中,如图所示,下列叙述错误的是( )
A.a中铁钉附近呈现蓝色沉淀
B.b中铁钉附近呈现红色
C.b中发生吸氧腐蚀
D.a中铜丝附近有气泡产生
【答案】B
【解析】A、a构成的是铁铜原电池,铁作为负极:Fe-2e-═Fe2+,与K3[Fe(CN)6]反应,生成蓝色沉淀,故A正确;
B、b中构成铁铝原电池,铝作负极,铁作正极,没有Fe3+ ,铁钉附近不可能呈现红色,故B错误;
C、正极上O2得电子,故 b中发生吸氧腐蚀,故C正确;
D、a中铜丝附近有气泡产生,H+ 得电子生成H2,故D正确。
故答案为:B
铁、铜作为原电池的电极时,铁做负极被氧化为亚铁离子,铝、铁作为原电池的电极时,铝做原电池的负极被氧化,结合电极反应进行分析即可.

 阅读快车系列答案
阅读快车系列答案【题目】“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请回答下列问题:
Ⅰ、(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成__________________。
(2)漂白粉的有效成分是________(均填化学式)。硅是无机非金属材料的主角,请你举出一种含硅的材料名称__________________。
(3)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是________________________________。
(4)高分子材料可以分成无机高分子材料和有机高分子材料。[AlFe(OH)n Cl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用生活用水和工业污水的处理,其中铁元素的化合价为________;
Ⅱ、高纯二氧化硅可用来制造光纤。某稻壳灰的成分为:
组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
通过如下流程可由稻壳灰制备较纯净的二氧化硅。
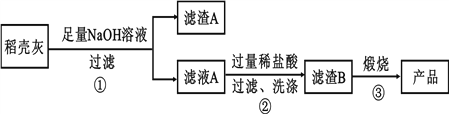
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是____________。
(2)步骤①中涉及SiO2的离子反应方程式为________________________________。
(3)滤渣A的成分有______________(填化学式)
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应