题目内容
【题目】【化学——选修2:化学与技术】
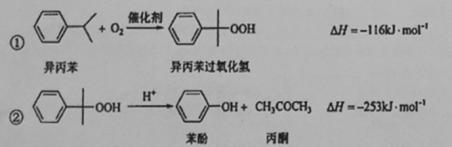
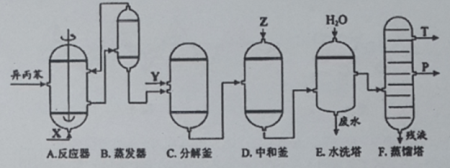
苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
相关化合物的物理常数
物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
异丙苯 | 120 | 0.8640 | 153 |
丙酮 | 58 | 0.7898 | 56.5 |
苯酚 | 94 | 1.0722 | 182 |
回答下列问题:
(1)在反应器A中通入的X是 。
(2)反应①和②分别在装置 和 中进行(填装置符号)。
(3)在分解釜C中加入的Y为少置浓硫酸,其作用是______,优点是用量少,缺点是_______________。
(4)反应②为 (填“放热”或“吸热”)反应。反应温度控制在50-60℃,温度过高的安全隐患是 。
(5)中和釜D中加入的Z最适宜的是 (填编号。已知苯酚是一种弱酸)。
a. NaOH b. CaCO3 c. NaHCO3 d. CaO
(6)蒸馏塔F中的馏出物T和P分别为 和 ,判断的依据是 。
(7)用该方法合成苯酚和丙酮的优点是 。
【答案】(1)氧气(或空气)
(2)A C
(3)催化剂(提高反应速率)腐蚀设备
(4)放热 可能会导致(过氧化物)爆炸
(5)c
(6)丙酮、苯酚;苯酚的沸点高于丙酮
(7)原子利用率高
【解析】
试题分析:(1)异丙苯被氧气氧化为异丙苯过氧化氢,异丙苯过氧化氢在酸性溶液中分解即可得到苯酚和丙酮,因此在反应器A中通入的X是氧气或空气。
(2)根据流程图可知反应①和②分别在装置A和C中进行。
(3)异丙苯过氧化氢在酸性溶液中分解,所以浓硫酸的作用是作催化剂,提高反应速率。由于浓硫酸具有酸性,因此缺点是容易腐蚀设备。
(4)△H小于0,则反应②为放热反应。反应温度控制在50~60℃,由于过氧化物受热易分解,因此温度过高的安全隐患是容易发生爆炸。
(5)苯酚与碳酸氢钠不反应,所以选择碳酸氢钠,答案选c。
(6)由于苯酚的沸点高于丙酮,丙酮先气化,所以蒸馏塔F中的馏出物T和P分别为丙酮和苯酚。
(7)根据反应的方程式以及以上分析可知用该方法合成苯酚和丙酮的优点是原子利用率高、没有副产物。