题目内容
将一定量由碳、氢、氧三种元素组成的有机化合物A的蒸气与3.2g氧气混合点燃,再将生成的气体依次通过①盛有浓硫酸的洗气瓶②灼热的氧化铜③饱和石灰水(设每个装置中的反应物均过量)。经测定①中增重3.60g ②中减重1.60g ③中增重8.80g。A蒸气的密度为3.393g/L(已换算成标准状况)。又测知既能与碳酸钠溶液反应又能与金属钠反应,且均有气体生成,但分别得到的气体在相同条件下体积不同。试求该有机物的分子式,并写出其可能的结构简式。
C2H4O3
解析:由题意知A的摩尔质量为3.393g·L-1![]() 22.4 L·mol-1 = 76g·mol-1。因为浓硫酸增重3.60g,所以可知一定量A中氢原子的物质的量:
22.4 L·mol-1 = 76g·mol-1。因为浓硫酸增重3.60g,所以可知一定量A中氢原子的物质的量: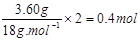 。由氧化铜减重可求知一氧化碳的物质的量:
。由氧化铜减重可求知一氧化碳的物质的量: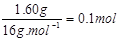 。由石灰水增重可求知二氧化碳的量:
。由石灰水增重可求知二氧化碳的量: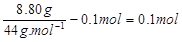 。根据原子守恒可知一定量A中氧原子的物质的量为:0.2mol+0.1mol+0.2mol-0.2mol=0.3mol。所以A的最简式为C2H4O3,由于式量为76,故其分子式为C2H4O3。根据A的性质可得出其结构简式为
。根据原子守恒可知一定量A中氧原子的物质的量为:0.2mol+0.1mol+0.2mol-0.2mol=0.3mol。所以A的最简式为C2H4O3,由于式量为76,故其分子式为C2H4O3。根据A的性质可得出其结构简式为。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目