题目内容
19.已知溶质质量分数为98%的浓硫酸(ρ=1.84g/mL),其物质的量浓度为18.4mol/L,取10mL该硫酸与amL水混合,配制成溶质质量分数为49%的硫酸溶液(ρ=1.40g/mL),其物质的量浓度为bmol/L.则a、b分别为( )| A. | a=10 b=9.2 | B. | a<10 b>9.2 | C. | a>10 b=9.2 | D. | a>10 b<9.2 |
分析 根据稀释过程中溶质硫酸的质量不变列方程计算加入水的体积a,结合c=$\frac{1000ρω}{M}$mol/L计算49%的硫酸的浓度,然后对各选项进行判断.
解答 解:稀释过程中溶质硫酸的质量不变,则:10mL×1.84g/mL×98%=(10mL×1.84g/mL+amL×1g/mL)×49%,解得a=18.4>10;
设49%的硫酸的密度为ρg/mL,硫酸浓度越大密度越大,则ρ<1.84,49%的硫酸的物质的量浓度b=$\frac{1000ρ×49%}{98}$mol/L=5ρ mol/L<9.2mol/L,
故选D.
点评 本题考查溶液浓度的有关计算,题目难度中等,注意掌握物质的量浓度与质量分数之间的关系,明确硫酸的浓度越大,则其密度越大.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
7.下列离子可能大量共存的是( )
| A. | 无色溶液:Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液:Na+、ClO?、SO42?、I? | |
| C. | 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- | |
| D. | 常温下,水电离出的c(H+)=1×10-13 mol•L-1的溶液:K+、Na+、Cl-、S2- |
4.下列化学用语正确的是( )
| A. | 乙烯的结构式:CH2=CH2 | B. | Clˉ的结构示意图: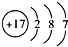 | ||
| C. | I-131:${\;}_{53}^{78}$I | D. | Na2S 的电子式: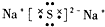 |
11.下列离子方程式正确的是( )
| A. | 向FeSO4溶液中加入少量Na2O2:4Na2O2+6H2O+4Fe2+═4Fe(OH)3↓+8Na++O2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀的质量最大:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 向NaClO溶液中通入少量SO2: 2ClO-+SO2+H2O═2HClO+SO32- | |
| D. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.4 mol/L的Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+2BaSO4↓+NH3•H2O |
8.NA代表阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 7.8g苯中碳碳双键的数目为0.3NA | |
| B. | 常温常压,11.2L CO和O2混合气体的原子数为NA | |
| C. | 1molNO2溶于足量水中,转移电子的数目为NA | |
| D. | 1.5g甲基所含有的电子数目为0.9NA |
9.把一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,则得反应后各物质的质量如下.下列说法中正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量(g) | 6.4 | 3.2 | 4.0 | 2.8 |
| 反应后的质量(g) | 5.2 | X | 7.2 | 2.8 |
| A. | a和c是反应物 | B. | d一定是催化剂 | ||
| C. | X=2.0g | D. | 该反应是化合反应 |

 .
.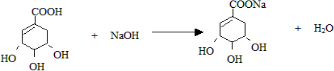 .
. -COOH),其反应类型是c
-COOH),其反应类型是c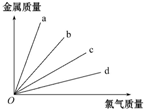 如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( )
如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( )