题目内容
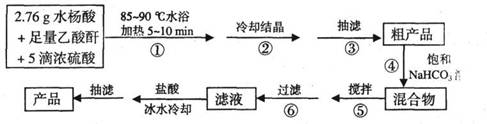
[实验化学]阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:

请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是
(2)写出制备阿司匹林的化学方程式
 .
.
(3)反应过程中,要控制温度在85℃~90℃,应采用的加热方法是
用这种方法加热需要的玻璃仪器有
(4)抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是
(5)如何检验产品中是否混有水杨酸?
 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是
防止乙酸酐水解
防止乙酸酐水解
.(2)写出制备阿司匹林的化学方程式


(3)反应过程中,要控制温度在85℃~90℃,应采用的加热方法是
水浴加热
水浴加热
.用这种方法加热需要的玻璃仪器有
酒精灯、烧杯、温度计
酒精灯、烧杯、温度计
.(4)抽滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是
关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物
关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物
.(5)如何检验产品中是否混有水杨酸?
向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸
向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸
.分析:(1)乙酸酐容易发生水解,故仪器应干燥;
(2)由水杨酸、乙酸酐与阿司匹林的结构可知,水杨酸中酚羟基中H原子与乙酸酐中-OCCH3交换,同时生成CH3COOH;
(3)控制温度在85℃~90℃,温度对于100℃,应采取水浴加热,所使用的玻璃仪器为:温度计、酒精灯、烧杯;
(4)用少量冰水洗涤方法是:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物;
(5)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,据此设计检验检验产品中是否混有水杨酸.
(2)由水杨酸、乙酸酐与阿司匹林的结构可知,水杨酸中酚羟基中H原子与乙酸酐中-OCCH3交换,同时生成CH3COOH;
(3)控制温度在85℃~90℃,温度对于100℃,应采取水浴加热,所使用的玻璃仪器为:温度计、酒精灯、烧杯;
(4)用少量冰水洗涤方法是:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物;
(5)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,据此设计检验检验产品中是否混有水杨酸.
解答:解:(1)乙酸酐容易发生水解生成乙酸,故仪器应干燥防止乙酸酐水解,
故答案为:防止乙酸酐水解;
(2)由水杨酸、乙酸酐与阿司匹林的结构可知,水杨酸中酚羟基中H原子与乙酸酐中-OCCH3交换,同时生成CH3COOH,反应方程式为: ,
,
故答案为: ;
;
(3)控制温度在85℃~90℃,小于100℃,应使用水浴加热,所用玻璃仪器有:酒精灯、烧杯、温度计;
故答案为:水浴加热;酒精灯、烧杯、温度计;
(4)用少量冰水洗涤方法是:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物,
故答案为:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物;
(5)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,具体方案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸,
故答案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸.
故答案为:防止乙酸酐水解;
(2)由水杨酸、乙酸酐与阿司匹林的结构可知,水杨酸中酚羟基中H原子与乙酸酐中-OCCH3交换,同时生成CH3COOH,反应方程式为:
 ,
,故答案为:
 ;
;(3)控制温度在85℃~90℃,小于100℃,应使用水浴加热,所用玻璃仪器有:酒精灯、烧杯、温度计;
故答案为:水浴加热;酒精灯、烧杯、温度计;
(4)用少量冰水洗涤方法是:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物,
故答案为:关闭水龙头,向布氏漏斗中加入冰水至浸没沉淀物,使冰水缓慢通过沉淀物;
(5)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,具体方案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸,
故答案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸.
点评:本题考查有机物的合成、实验基本操作、物质的分离提纯、实验方案设计等,题目难度不大,注意掌握基本操作与有机物的性质.

练习册系列答案
相关题目


 (3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。
(3)乙二胺分子中氮原子轨道的杂化类型为_____________。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_______________________________________。



 (4)②中所形成的配离子中含有的化学键类型有__________。(填字母)
(4)②中所形成的配离子中含有的化学键类型有__________。(填字母)


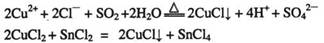

 (4)②中所形成的配离子中含有的化学键类型有__________。(填字母)
(4)②中所形成的配离子中含有的化学键类型有__________。(填字母)