题目内容
有硫酸与硝酸的混合液,取出其中10ml,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为9.32g.另取这种溶液10ml与4mol/L的NaOH溶液25ml恰好中和。
小题1:求混合液中H2SO4与HNO3的物质的量浓度是多少?
小题2:另取10ml的混合液与0.96g铜粉共热时,有多少ml气体产生?
小题1:求混合液中H2SO4与HNO3的物质的量浓度是多少?
小题2:另取10ml的混合液与0.96g铜粉共热时,有多少ml气体产生?
小题1:c(H2SO4)=4mol/L,c(HNO3) =2moL/L
小题2:V(NO)=0.224L
小题1:由题意知硫酸钡的物质的量:n(BaSO4)=n(H2SO4)=" 9.32g/233g/moL=0.04mol," 溶液中的H+与NaOH反应,n(NaOH)=n(H+)=0.025L×4mol/L="0.1mol, " n(HNO3)=0,1mol-2 n(H2SO4)="=" 0.02mol, c(H2SO4)=4mol/L,c(HNO3) ="2moL/L"
小题2:溶液中的n(H+)=0.04×2+0.02="0.10mol," n(HNO3)=0.02mol,n(Cu)=0.015mol,由化学反应3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,因此与0.015mol的Cu反应需要的H+的物质的量为0.04mol<0. 1mol同理反应掉的NO3-的物质的量为0.01mol<0.02mol,所以H+与NO3-均过量,Cu全部溶解,生成的NO的体积应据Cu的物质的量来计算,即n(NO)=2/3×0.015=0.01mol,所以V(NO)="0.224L."

练习册系列答案
相关题目
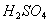 、
、 三种物质的混合溶液,已知在该混合液中,
三种物质的混合溶液,已知在该混合液中,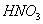 和
和 不同的比值范围内,参加反应的Cu的质量。
不同的比值范围内,参加反应的Cu的质量。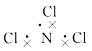
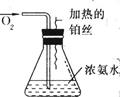
 N2(g)+3H2O(l) 2NH3(g)+
N2(g)+3H2O(l) 2NH3(g)+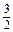 O2(g)
O2(g)
 (3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入
(3)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入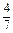 。计算:
。计算: ②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。
②该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。