题目内容
能正确表示下列反应的离子方程式的是( )
A.将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++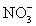 =Fe3++2H2O+NO↑
=Fe3++2H2O+NO↑
D.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
A
【解析】A正确,符合3个守恒;B错误,电荷不守恒,Fe3O4中Fe有两种价态,正确的离子方程式应该为:Fe3O4+8H+=2Fe3++Fe2++4H2O;C错误,得失电子不守恒,电荷不守恒,正确的离子方程式应为:3Fe2++ +4H+=3Fe3++NO↑+2H2O;D错误,不符合客观实际,反应后只能生成Fe2+和H2。
+4H+=3Fe3++NO↑+2H2O;D错误,不符合客观实际,反应后只能生成Fe2+和H2。

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目



