��Ŀ����
����Ŀ��ij����С�齫��ͼ��ʾװ�ð�һ��˳�����ӣ���ʵ��������ȡһ������FeCl3����ͨ�����������ַ�Ӧ������ش��������⣺
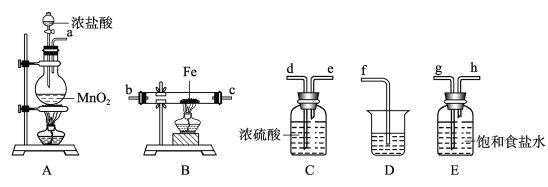
��1��A�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________��
��2����װ�õ���ȷ����˳��Ϊ����дװ�ô��ţ�A��_______��_______��_______��D��
��3��װ��E��������___________________��д��װ��D(D����ʢ��ҺΪKOH)�з�Ӧ�Ļ�ѧ����ʽ___________________
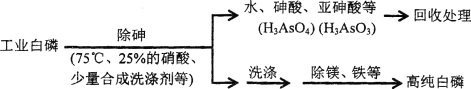
��4����ҵ�����������ķ���ʽΪ________________________��
��5�����ŷ�Ӧ�Ľ��У����ַ�Һ©���е�Ũ�����β���ȥ����ԭ����________________��
���𰸡���1��MnO2+4HCl��Ũ��![]() MnCl2+Cl2�� +2H2O
MnCl2+Cl2�� +2H2O
��2��E��C��B
��3����ȥ�����л��е�HCl
2KOH+Cl2=KCl+KClO+H2O
��4��![]()
��5�����Ų����������������࣬Բ����ƿ�ڵ�ѹǿ�������Է�Һ©���ڵ�Ũ�������Ե���
��������
�����������1��A������Ũ������MnO2��Ӧ��ȡCl2����Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��![]() MnCl2+Cl2�� +2H2O����2��װ��A��ȡ����������HCl��H2O�������ʣ�����Fe��Ӧ֮ǰ��������Ҫ���������������ͨ��װ��E���Ҵ�g��h�����Գ�ȥ��������е�HCl���ʣ�����������ͨ��װ��C��d��e�����Գ�ȥ��������е�H2O����e�������Ǵ���������������ͨ��װ��B����������Fe��Ӧ��ȡFeCl3���������������������Һ����β������ֹ��Ⱦ�������ʸ�װ�õ�����˳��Ϊ��A��E��C��B��D����3��װ��E�������dz�ȥ�����л��е�HCl��KOH�ܹ���������Ӧ������ʽΪ2KOH+Cl2=KCl+KClO+H2O����4����ҵ�����õ�ⱥ�͵�ʳ��ˮ����ȡ��������Ӧ�ķ���ʽΪ��
MnCl2+Cl2�� +2H2O����2��װ��A��ȡ����������HCl��H2O�������ʣ�����Fe��Ӧ֮ǰ��������Ҫ���������������ͨ��װ��E���Ҵ�g��h�����Գ�ȥ��������е�HCl���ʣ�����������ͨ��װ��C��d��e�����Գ�ȥ��������е�H2O����e�������Ǵ���������������ͨ��װ��B����������Fe��Ӧ��ȡFeCl3���������������������Һ����β������ֹ��Ⱦ�������ʸ�װ�õ�����˳��Ϊ��A��E��C��B��D����3��װ��E�������dz�ȥ�����л��е�HCl��KOH�ܹ���������Ӧ������ʽΪ2KOH+Cl2=KCl+KClO+H2O����4����ҵ�����õ�ⱥ�͵�ʳ��ˮ����ȡ��������Ӧ�ķ���ʽΪ��![]() ����5�����ŷ�Ӧ�Ľ��У����ַ�Һ©���е�Ũ�����β���ȥ����ԭ�������Ų����������������࣬Բ����ƿ�ڵ�ѹǿ����ʹ�÷�Һ©���ڵ�Ũ�������Ե��¡�
����5�����ŷ�Ӧ�Ľ��У����ַ�Һ©���е�Ũ�����β���ȥ����ԭ�������Ų����������������࣬Բ����ƿ�ڵ�ѹǿ����ʹ�÷�Һ©���ڵ�Ũ�������Ե��¡�