题目内容
17gNH3共有 mol电子,0.1molH2S共有约 个原子,同温同压下,同体积的NH3和H2S气体的质量比为 .
【答案】分析:根据n=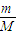 计算17gNH3的物质的量,氨气分子中含有10个电子,故电子的物质的量为氨分子的10倍;
计算17gNH3的物质的量,氨气分子中含有10个电子,故电子的物质的量为氨分子的10倍;
H2S分子中含有3个原子,原子的物质的量为H2S的3倍,再根据N=nNA计算原子的数目;
同温同压下,同体积的NH3和H2S气体的物质的量相同,根据m=nM可知,质量之比等于摩尔质量之比.
解答:解:17gNH3的物质的量为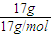 =1mol,氨气分子中含有10个电子,电子的物质的量为1mol×10=10mol,
=1mol,氨气分子中含有10个电子,电子的物质的量为1mol×10=10mol,
H2S分子中含有3个原子,原子的物质的量为H2S的3倍,故0.1molH2S含有原子的物质的量为0.1mol×3=0.3mol,含有的原子的数目为0.3mol×NAmol-1=0.3NA,
同温同压下,同体积的NH3和H2S气体的物质的量相同,根据m=nM可知,NH3和H2S气体的质量之比等于摩尔质量之比为17g/mol:24g/mol=1:2,
故答案为:10;0.3NA;1:2.
点评:本题考查常用化学计量的有关计算等,注意对公式的理解与灵活运用,题目难度不大.
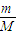 计算17gNH3的物质的量,氨气分子中含有10个电子,故电子的物质的量为氨分子的10倍;
计算17gNH3的物质的量,氨气分子中含有10个电子,故电子的物质的量为氨分子的10倍;H2S分子中含有3个原子,原子的物质的量为H2S的3倍,再根据N=nNA计算原子的数目;
同温同压下,同体积的NH3和H2S气体的物质的量相同,根据m=nM可知,质量之比等于摩尔质量之比.
解答:解:17gNH3的物质的量为
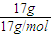 =1mol,氨气分子中含有10个电子,电子的物质的量为1mol×10=10mol,
=1mol,氨气分子中含有10个电子,电子的物质的量为1mol×10=10mol,H2S分子中含有3个原子,原子的物质的量为H2S的3倍,故0.1molH2S含有原子的物质的量为0.1mol×3=0.3mol,含有的原子的数目为0.3mol×NAmol-1=0.3NA,
同温同压下,同体积的NH3和H2S气体的物质的量相同,根据m=nM可知,NH3和H2S气体的质量之比等于摩尔质量之比为17g/mol:24g/mol=1:2,
故答案为:10;0.3NA;1:2.
点评:本题考查常用化学计量的有关计算等,注意对公式的理解与灵活运用,题目难度不大.

练习册系列答案
相关题目