题目内容
(2011?如皋市模拟)二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能.
Ⅰ.工业制备二甲醚的生产流程如下:
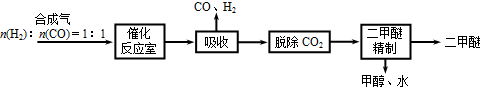
催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
(1)甲烷氧化可制合成气:CH4(g)+
O2(g)?CO(g)+2H2(g)△H=-35.6kJ/mol,该反应是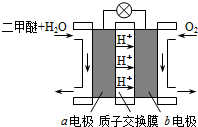
(2)催化反应室中总反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的△H=
(3)上述流程中,可循环使用的物质有
Ⅱ.如图为绿色电源“直接二甲醚燃料电池”的工作原理示意图.
(1)b电极是
(2)a电极的反应式为
Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
(1)甲烷氧化可制合成气:CH4(g)+
| 1 | 2 |
自发
自发
反应(填“自发”或“非自发”).
(2)催化反应室中总反应3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)的△H=
-246.1kJ/mol
-246.1kJ/mol
.830℃时反应③的K=1.0,则在催化反应室中反应③的K>
>
1.0(填“>”、“<”或“=”)(3)上述流程中,可循环使用的物质有
CO、H2、甲醇和水
CO、H2、甲醇和水
.Ⅱ.如图为绿色电源“直接二甲醚燃料电池”的工作原理示意图.
(1)b电极是
正
正
极.(2)a电极的反应式为
(CH3)2O-12e-+3H2O═2CO2+12H+
(CH3)2O-12e-+3H2O═2CO2+12H+
.分析:Ⅰ、(1)依据自发进行的判断依据为△H-T△S<0,是自发进行的反应;△H-T△S>0,是非自发进行的反应;
(2)依据热化学方程式和盖斯定律计算得到热化学方程式进行计算应用;催化反应室内的反应条件是压力2.0~10.0Mpa,温度230~280℃;结合化学平衡影响因素分析判断;
(3)依据反应过程中的中间产物是可以循环利用的物质;
Ⅱ、反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,正极反应还原反应,b为正极,氧气在正极放电.由图可知,a极为负极,二甲醚放电生成二氧化碳与氢离子.
(2)依据热化学方程式和盖斯定律计算得到热化学方程式进行计算应用;催化反应室内的反应条件是压力2.0~10.0Mpa,温度230~280℃;结合化学平衡影响因素分析判断;
(3)依据反应过程中的中间产物是可以循环利用的物质;
Ⅱ、反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,正极反应还原反应,b为正极,氧气在正极放电.由图可知,a极为负极,二甲醚放电生成二氧化碳与氢离子.
解答:解:I.(1)甲烷氧化可制合成气:CH4(g)+
O2(g)?CO(g)+2H2(g)△H=-35.6kJ/mol,△S>0,△H<0,;△H-T△S<0,反应能自发进行,故答案为:自发;
(2)催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应.
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
依据盖斯定律①×2+②+③得到:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=-246.1kJ/mol;
830℃时反应③的K=1.0,则在催化反应室中,压力2.0~10.0Mpa,温度230~280℃,温度降低.平衡正向进行,反应③的K增大;
故答案为:-246.1kJ/mol;>;
(3)依据催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应.
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
CO、甲醇和水,是中间产物,H2也可以部分循环,故答案为:CO、H2、甲醇和水;
II.反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,正极反应还原反应,氧气在正极放电.由图可知,a极为负极,二甲醚放电生成二氧化碳与氢离子,a电极的电极反应式为 CH3OCH3-12e-+3H2O=2CO2+12H+,b为正极,氧气得到电子发生还原反应,故答案为:正;CH3OCH3+3H2O-12e-=2CO2+12H+.
| 1 |
| 2 |
(2)催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应.
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
依据盖斯定律①×2+②+③得到:3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H=-246.1kJ/mol;
830℃时反应③的K=1.0,则在催化反应室中,压力2.0~10.0Mpa,温度230~280℃,温度降低.平衡正向进行,反应③的K增大;
故答案为:-246.1kJ/mol;>;
(3)依据催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应.
①CO(g)+2H2(g)?CH3OH(g)△H=-90.7kJ/mol
②2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol
③CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.2kJ/mol
CO、甲醇和水,是中间产物,H2也可以部分循环,故答案为:CO、H2、甲醇和水;
II.反应本质是二甲醚的燃烧,原电池负极发生氧化反应,二甲醚在负极放电,正极反应还原反应,氧气在正极放电.由图可知,a极为负极,二甲醚放电生成二氧化碳与氢离子,a电极的电极反应式为 CH3OCH3-12e-+3H2O=2CO2+12H+,b为正极,氧气得到电子发生还原反应,故答案为:正;CH3OCH3+3H2O-12e-=2CO2+12H+.
点评:本题考查了反应自发进行的判断依据,盖斯定律的计算应用,平衡影响因素的分析判断,原电池的电极判断,电极反应书写应用,题目难度中等.

练习册系列答案
相关题目
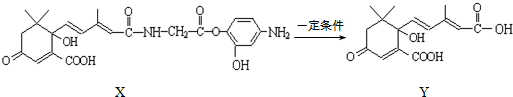
 、④HCHO等,其中碳原子采取sp2杂化的分子有
、④HCHO等,其中碳原子采取sp2杂化的分子有
