题目内容
硫酸锌是一种重要的工业原料.在实验室从粗锌(含有少量的铅)与稀硫酸反应后的废液中提取硫酸锌的主要操作步骤如下:
步骤1:将废液过滤,调节滤液的pH约为2,过滤,将滤液加热浓缩,制得较高温度下的饱和溶液,冷却结晶得到粗制晶体.
步骤2:①在烧杯中用蒸馏水溶解步骤1得到的晶体,滴加少量稀硫酸,水浴加热至晶体全部溶解.②停止加热,让其自然冷却、结晶.③抽滤,用少量无水乙醇洗涤晶体1~2次,得精制晶体.
(1)废液中含有的不溶性杂质是 .
(2)步骤1中调节滤液pH约为2,可加入的物质是 .(填字母)
a.NH3?H2O b.ZnO c.ZnCO3 d.NaOH
(3)步骤1中对滤液加热浓缩时,当 时,停止加热.
(4)步骤2中滴加少量稀硫酸的目的是 .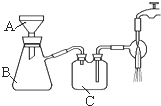
(5)抽滤装置如图所示,仪器B的名称是 .仪器C的作用是 .
(6)用少量无水乙醇洗涤晶体的目的是 .
步骤1:将废液过滤,调节滤液的pH约为2,过滤,将滤液加热浓缩,制得较高温度下的饱和溶液,冷却结晶得到粗制晶体.
步骤2:①在烧杯中用蒸馏水溶解步骤1得到的晶体,滴加少量稀硫酸,水浴加热至晶体全部溶解.②停止加热,让其自然冷却、结晶.③抽滤,用少量无水乙醇洗涤晶体1~2次,得精制晶体.
(1)废液中含有的不溶性杂质是
(2)步骤1中调节滤液pH约为2,可加入的物质是
a.NH3?H2O b.ZnO c.ZnCO3 d.NaOH
(3)步骤1中对滤液加热浓缩时,当
(4)步骤2中滴加少量稀硫酸的目的是

(5)抽滤装置如图所示,仪器B的名称是
(6)用少量无水乙醇洗涤晶体的目的是
分析:(1)PbSO4不溶于水;
(2)除杂不能引入新的杂质;
(3)蒸发时不能蒸干;
(4)锌离子易发生水解;
(5)根据仪器形状确定名称,C可防止倒吸;
(6)乙醇易挥发.
(2)除杂不能引入新的杂质;
(3)蒸发时不能蒸干;
(4)锌离子易发生水解;
(5)根据仪器形状确定名称,C可防止倒吸;
(6)乙醇易挥发.
解答:解:(1)不溶性杂质是PbSO4,故答案为:PbSO4;
(2)ZnO、ZnCO3可与硫酸反应调节pH值,且不引入新的杂质,故答案为:bc;
(3)蒸发时不能蒸干,当溶液表面出现晶膜时停止加热,故答案为:溶液表面出现晶膜;
(4)锌离子易发生水解,加入硫酸防止硫酸锌水解,故答案为:防止硫酸锌水解;
(5)B为吸滤瓶,仪器C可防止倒吸,故答案为:吸滤瓶;防止倒吸;
(6)乙醇易挥发,可将水分带走,故答案为:利用乙醇挥发性除去晶体表面的水分.
(2)ZnO、ZnCO3可与硫酸反应调节pH值,且不引入新的杂质,故答案为:bc;
(3)蒸发时不能蒸干,当溶液表面出现晶膜时停止加热,故答案为:溶液表面出现晶膜;
(4)锌离子易发生水解,加入硫酸防止硫酸锌水解,故答案为:防止硫酸锌水解;
(5)B为吸滤瓶,仪器C可防止倒吸,故答案为:吸滤瓶;防止倒吸;
(6)乙醇易挥发,可将水分带走,故答案为:利用乙醇挥发性除去晶体表面的水分.
点评:本题考查物质的分离、提纯和除杂,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 抽滤装置如图所示,仪器B的名称是 ▲ 。仪器C的作用是 ▲ 。
抽滤装置如图所示,仪器B的名称是 ▲ 。仪器C的作用是 ▲ 。

