题目内容
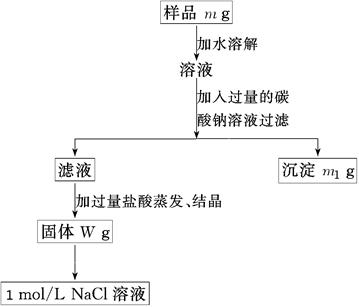
(8分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
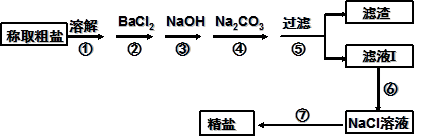
请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是 ,所需要的实验仪器和用品除铁架台、酒精灯、玻璃棒外,还要 。
(2)步骤③加入过量NaOH的目的是:
(3)步骤⑥需加入适量的 (填试剂名称),所发生反应的离子方程式为:
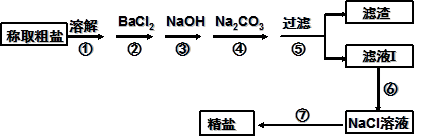
请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是 ,所需要的实验仪器和用品除铁架台、酒精灯、玻璃棒外,还要 。
(2)步骤③加入过量NaOH的目的是:
(3)步骤⑥需加入适量的 (填试剂名称),所发生反应的离子方程式为:
(1)蒸发, 蒸发皿; (2)溶液中存在的 Mg2+ 和 Fe3+完全转化为沉淀除去。
(3)盐酸 OH-+H+= H2O CO32-+2H+=H2O+CO2
(3)盐酸 OH-+H+= H2O CO32-+2H+=H2O+CO2
试题分析:(1)由溶液变成晶体的操作叫蒸发,需要用的一起除铁架台、酒精灯、玻璃棒外,还要蒸发皿。
(2)步骤③加入过量NaOH的目的是溶液中存在的 Mg2+ 和 Fe3+完全转化为沉淀除去。
(3)滤液I中还有大量的OH-、CO32-杂质离子,所以需要加盐酸除去。发生的离子方程式为:OH-+H+=H2O CO32-+2H+=H2O+CO2
点评:把物质中混有的杂质除去而获得纯净物叫提纯,将相互混在一起的不同物质彼此分开而得到相应组分的各纯净物叫分离。在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。

练习册系列答案
相关题目