题目内容
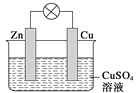
【题目】在铜锌原电池中,以硫酸铜为电解质溶液,锌为________极,电极上发生的是________(填“氧化”或“还原”)反应,电极反应式为___________。
锌片上观察到的现象为________;铜为________极,电极上发生的是________(填“氧化”或“还原”)反应,电极反应式是________;铜片上观察到的现象是________
【答案】 负 氧化 Zn-2e-===Zn2+ 锌片溶解 正 还原 Cu2++2e-===Cu 铜极变粗
【解析】本题考查原电池的工作原理,由于锌比铜活泼,发生Zn+Cu2+=Zn2++Cu,根据原电池工作原理,负极上发生氧化反应,失去电子,即锌作负极,电极反应式为Zn-2e-=Zn2+,观察到锌片溶解,铜为正极,电极反应式为Cu2++2e-=Cu,化合价降低,发生还原反应,铜片上现象:铜极变粗。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目