题目内容
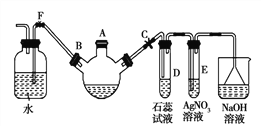
【题目】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。已知碱石灰的成分是氢氧化钠和氧化钙的混合物;炭与水蒸气在高温条件下发生以下反应:C + H2O(g)![]() CO + H2。回答下列问题:
CO + H2。回答下列问题:
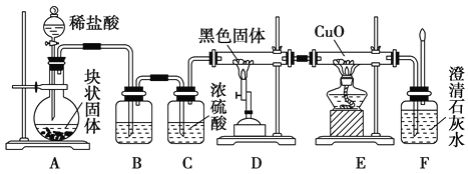
(1)写出装置A中发生反应的离子方程式____________________。
(2)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是:____________。
(3)装置D中黑色固体为___________ (填名称)。
(4)按照如图装置进行实验时,首先进行的操作是___________________________________ 。
(5)根据实验中的____________________________现象,可证明CO具有还原性。
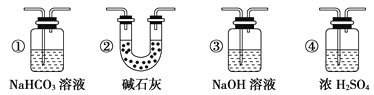
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置____与____之间连接下图中的____________________装置(填序号)。
【答案】CaCO3+2H+=Ca2++H2O+CO2↑ 没有除去气体中的水蒸气,高温下水蒸气与碳反应生成H2和CO,H2也能还原CuO 炭 检查装置的气密性 E装置中黑色固体变成红色 D E ②
【解析】
(1)装置A中是盐酸和石灰石反应生成二氧化碳、氯化钙和水,其反应离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑;
(2)实验室用盐酸和石灰石制取二氧化碳,该反应放出的热量导致盐酸挥发,所以制取的二氧化碳中含有氯化氢气体,为除去氯化氢气体,选取的试剂应能除去氯化氢气体且不和二氧化碳反应,则只能选取可溶性的饱和碳酸氢盐,一般常用饱和的碳酸氢钠溶液,即B中试剂是饱和碳酸氢钠溶液;然后通过浓硫酸干燥二氧化碳,若实验中没有装置C,使装置B与装置D直接相连,即二氧化碳没有干燥,根据已知信息可知高温下水蒸气能与碳反应生成氢气和CO,由于H2也能还原CuO,因此会对实验造成影响;
(3)高温条件下,二氧化碳和碳反应生成一氧化碳,所以D装置中的黑色固体是炭;
(4)在做与气体有关的实验操作时,连接完仪器以后,加药品前,首先要检验装置的气密性,以免装置气密性不好,气体泄漏污染空气;
(5)一氧化碳具有还原性,所以能还原黑色的氧化铜,使其变为红色的铜单质,因此根据实验中的E装置中黑色固体变成红色现象,可证明CO具有还原性;
(6)碳和二氧化碳的反应中,二氧化碳不可能完全转化为一氧化碳,所以从D装置出来的气体中含有二氧化碳,为防止原来二氧化碳的干扰,应先把D出来的二氧化碳除去,再将一氧化碳气体通过E装置,二氧化碳是酸性氧化物,所以用碱性物质除去,所以应在上图装置D与E之间连接装置②。

 黄冈创优卷系列答案
黄冈创优卷系列答案【题目】组成生命的最基本元素之一是碳,其单质及化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子价电子原子轨道表示式为________,其核外有________种空间运动状态的电子.
(2) 有机物中都含有碳原子,这和碳原子电子云的成键特点有关,试解释有机物种类繁多的原因________ 。
(3) 比较下列碳酸盐在一定温度下会发生分解的温度和对应的阳离子半径,分析其变化规律及原因_____________。
碳酸盐 | MgCO3 | CaCO3 | BaCO3 | SrCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
阳离了半径/pm | 66 | 99 | 112 | 135 |
(4)1828 年,德国化学家乌勒(F·Wohler)冲破了生命力学说的束缚,在实验室里将无机物氰酸铵(NH4CNO)溶液蒸发,得到了有机物尿素[CO(NH2)2]。尿素中C、N、O第一电离能大小顺序为____________。
(5) 碳的同素异形体有多种,其中一种为石墨,系平面层状结构。同一层内每个碳原子与其它三个碳原子以C -C 键相连构成平面正六边形,且层间可以滑动,它的结构如图所示。其中碳原子的杂化方式为_______,层间存在的作用力为__________。
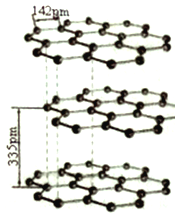
(6)石墨晶体二维结构的特殊性。
①同一层面内的平面六元并环结构(见上图)。在含lmolC原子的石墨中,有_____个平面正六边形。
②已知石墨层间距为335pm,C-C键长为142pm,其密度______g/cm3(已知:lpm=10-10cm。列出计算式即可)