题目内容
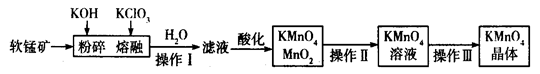
工业上用软锰矿(主要成分为MnO2)制备高锰酸钾的工艺流程如图所示:
(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。下列 酸能用于酸化高锰酸钾溶液的是____________(填序号)。
(2)操作Ⅰ、Ⅱ、Ⅲ的名称分别是______________、_______________、_______________。
(3)软锰矿与过量固体KOH和KClO3在熔融状态下反应时的氧化剂是__________________(填化学式)。反应后加水溶解得到的滤液中主要含有KCl和K2MnO4,则滤液酸化时发生反应的离子方程式为 _______________________________。
(4)已知KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2。取上述制得的KMnO4产品0.33 g,恰好与0.67 g Na2C2O4完全反应,则KMnO4的纯度为________%。

(1)高锰酸钾的氧化性强弱与溶液的酸碱性有关,在酸性条件下其氧化性较强。下列 酸能用于酸化高锰酸钾溶液的是____________(填序号)。
| A.盐酸 | B.稀硫酸 | C.硝酸 | D.氢硫酸 |
(3)软锰矿与过量固体KOH和KClO3在熔融状态下反应时的氧化剂是__________________(填化学式)。反应后加水溶解得到的滤液中主要含有KCl和K2MnO4,则滤液酸化时发生反应的离子方程式为 _______________________________。
(4)已知KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2。取上述制得的KMnO4产品0.33 g,恰好与0.67 g Na2C2O4完全反应,则KMnO4的纯度为________%。
(10分)
(1)b (1分)
(2) 过滤(1分) 过滤(1分) 蒸发(1分)
(3)KClO3(1分);3MnO42-+4H+=2MnO4-+MnO2↓+2H2O(2分)
(4)96(3分)
(1)b (1分)
(2) 过滤(1分) 过滤(1分) 蒸发(1分)
(3)KClO3(1分);3MnO42-+4H+=2MnO4-+MnO2↓+2H2O(2分)
(4)96(3分)
 试题分析:(1)高锰酸钾能氧化盐酸和氢硫酸,硝酸本身具有强氧化性,故选硫酸;(2) 由进行操作Ⅰ后得滤液,故操作Ⅰ应为过滤,由于MnO2难溶于水操作Ⅱ后得KMnO4溶液,故操作Ⅱ为过滤,进行操作Ⅲ后使溶液变成了晶体,故操作Ⅲ为蒸发;(3)由产物及元素的化合价可知氧化剂应为KClO3,滤液中主要成分是K2MnO4,酸化后得到KMnO4和MnO2,故方程式为:3MnO42-+4H+=2MnO4-+MnO2↓+2H2O;(4)由题意及电子守恒可得关系式为:
试题分析:(1)高锰酸钾能氧化盐酸和氢硫酸,硝酸本身具有强氧化性,故选硫酸;(2) 由进行操作Ⅰ后得滤液,故操作Ⅰ应为过滤,由于MnO2难溶于水操作Ⅱ后得KMnO4溶液,故操作Ⅱ为过滤,进行操作Ⅲ后使溶液变成了晶体,故操作Ⅲ为蒸发;(3)由产物及元素的化合价可知氧化剂应为KClO3,滤液中主要成分是K2MnO4,酸化后得到KMnO4和MnO2,故方程式为:3MnO42-+4H+=2MnO4-+MnO2↓+2H2O;(4)由题意及电子守恒可得关系式为:2KMnO4~5NaC2O4
2×158 5×134
m 0.67g
解得m=0.316g
KMnO4的纯度为0.316/0.33×100%=86%

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 ,依次加入的物质可以是
,依次加入的物质可以是 溶液、
溶液、 溶液和盐酸
溶液和盐酸