题目内容
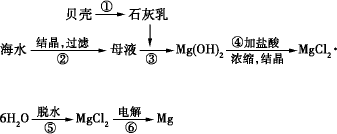
从海水中提取镁的工艺流程可表示如下:

下列说法不正确的是
- A.用此法提取镁的优点之一是原料来源丰富
- B.步骤⑥电解MgCl2时阴极产生氯气
- C.步骤⑤可将晶体置于HCl气体氛围中脱水
- D.上述工艺流程中涉及化合、分解和复分解反应
B
海水中含有大量的镁元素,从海水中提取镁的优点之一是原料来源丰富,选项A正确;电解熔融的MgCl2时,阳极产生Cl2,阴极产生金属镁,选项B错误;因MgCl2能水解:MgCl2+2H2O Mg(OH)2+2HCl,所以将MgCl2·6H2O晶体在HCl气体氛围中加热脱水,其目的是防止MgCl2水解生成Mg(OH)2,选项C正确;步骤①涉及CaCO3的分解反应得到CaO,CaO与H2O发生化合反应得到Ca(OH)2,步骤⑥是电解涉及分解反应,步骤③涉及MgCl2与Ca(OH)2发生复分解反应得到Mg(OH)2和CaCl2。
Mg(OH)2+2HCl,所以将MgCl2·6H2O晶体在HCl气体氛围中加热脱水,其目的是防止MgCl2水解生成Mg(OH)2,选项C正确;步骤①涉及CaCO3的分解反应得到CaO,CaO与H2O发生化合反应得到Ca(OH)2,步骤⑥是电解涉及分解反应,步骤③涉及MgCl2与Ca(OH)2发生复分解反应得到Mg(OH)2和CaCl2。
海水中含有大量的镁元素,从海水中提取镁的优点之一是原料来源丰富,选项A正确;电解熔融的MgCl2时,阳极产生Cl2,阴极产生金属镁,选项B错误;因MgCl2能水解:MgCl2+2H2O
 Mg(OH)2+2HCl,所以将MgCl2·6H2O晶体在HCl气体氛围中加热脱水,其目的是防止MgCl2水解生成Mg(OH)2,选项C正确;步骤①涉及CaCO3的分解反应得到CaO,CaO与H2O发生化合反应得到Ca(OH)2,步骤⑥是电解涉及分解反应,步骤③涉及MgCl2与Ca(OH)2发生复分解反应得到Mg(OH)2和CaCl2。
Mg(OH)2+2HCl,所以将MgCl2·6H2O晶体在HCl气体氛围中加热脱水,其目的是防止MgCl2水解生成Mg(OH)2,选项C正确;步骤①涉及CaCO3的分解反应得到CaO,CaO与H2O发生化合反应得到Ca(OH)2,步骤⑥是电解涉及分解反应,步骤③涉及MgCl2与Ca(OH)2发生复分解反应得到Mg(OH)2和CaCl2。 
练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目