题目内容
某含铬Cr2O2-7废水用硫酸亚铁铵[FeSO4?(NH4)2SO4?6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀干燥后得到nmol FeO?FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是
- A.消耗硫酸亚铁铵的物质的量为n(3x+l)mol
- B.处理废水中Cr2O72-的物质的量为
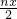 mo1
mo1 - C.反应中发生转移的电子的物质的量为6nx mol
- D.在FeO?FeyCrxO3中3x=y
C
分析:A.由铁元素守恒,求出消耗硫酸亚铁的物质的量,结合电子转移守恒或FeO?FeyCrxO3电中性找出x与y,代入硫酸亚铁的物质的量计算;
B.反应的铬元素完全转化为沉淀,根据铬原子守恒计算;
C.Cr2O72-中Cr为+6价,被还原为+3价Cr,每个Cr原子得3个电子,计算出Cr原子物质的量,转移电子为Cr原子物质的量3倍;
D.根据失电子守恒计算.
解答:A.由铁元素守恒,消耗硫酸亚铁铵的物质的量为n(y+1),又由FeO?FeyCrxO3电中性知3x+3y=6,代入前式得,消耗硫酸亚铁铵的物质的量为n(3-x);或由得失电子守恒得3x=y,代入得n×(1+y)mol=n×(3x+1)mol,故A正确;
B.根据铬原子守恒,Cr原子为nxmol,故Cr2O72-的物质的量为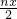 mol,故B正确;
mol,故B正确;
C.得到nmolFeO?FeyCrxO3,则一共有nxmolCr原子参加反应,1molCr转移电子3mol,故转移的电子数为3nxmol,故C错误;
D、FeO?FeyCrxO3中,Fe为正三价,由得失电子守恒知3x-y=0,即3x=y,故D正确.
故选C.
点评:本题考查氧化还原反应,题目难度中等,注意原子守恒、电子守恒在计算中的应用,使计算简单化.
分析:A.由铁元素守恒,求出消耗硫酸亚铁的物质的量,结合电子转移守恒或FeO?FeyCrxO3电中性找出x与y,代入硫酸亚铁的物质的量计算;
B.反应的铬元素完全转化为沉淀,根据铬原子守恒计算;
C.Cr2O72-中Cr为+6价,被还原为+3价Cr,每个Cr原子得3个电子,计算出Cr原子物质的量,转移电子为Cr原子物质的量3倍;
D.根据失电子守恒计算.
解答:A.由铁元素守恒,消耗硫酸亚铁铵的物质的量为n(y+1),又由FeO?FeyCrxO3电中性知3x+3y=6,代入前式得,消耗硫酸亚铁铵的物质的量为n(3-x);或由得失电子守恒得3x=y,代入得n×(1+y)mol=n×(3x+1)mol,故A正确;
B.根据铬原子守恒,Cr原子为nxmol,故Cr2O72-的物质的量为
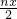 mol,故B正确;
mol,故B正确; C.得到nmolFeO?FeyCrxO3,则一共有nxmolCr原子参加反应,1molCr转移电子3mol,故转移的电子数为3nxmol,故C错误;
D、FeO?FeyCrxO3中,Fe为正三价,由得失电子守恒知3x-y=0,即3x=y,故D正确.
故选C.
点评:本题考查氧化还原反应,题目难度中等,注意原子守恒、电子守恒在计算中的应用,使计算简单化.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
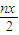 mo1
mo1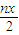 mo1
mo1