题目内容
在N2+3H2A.v(H2)=0.7 mol·(L·min)–1
B.v(NH3)=0.3 mol·(L·min)-1
C.v(H2)=0.2 mol·(L·min)-1
D.v(H2)=0.15 mol·(L·min)-1
D
解析: N2 + 3H2![]() 2NH3
2NH3
起始浓度/mol·L 3 4 0.5
3 min后浓度/mol·L 0.8
变化浓度/mol·L 0.15 0.45 0.3
化学反应速率的计算要掌握基本格式,以上所列,还应掌握起始浓度和某时刻后浓度的关系,即:
[反应物]减小=[反应物]起始-[反应物]某时刻
[生成物]增加=[生成物]某时刻-[生成物]起始
所以分别求得:v(N2)=0.05 mol·L·min,v(H2)=0.15 mol·(L·min),
v(NH3)=0.1 mol·(L·min)。

练习册系列答案
相关题目
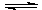 2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol·L-1,在此时间内用H2表示的反应速率为0.45mol·L-1·s-1,则该反应所经历的时间是( )
2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol·L-1,在此时间内用H2表示的反应速率为0.45mol·L-1·s-1,则该反应所经历的时间是( )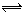 2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,在此时间内用H2表示的平均反应速率为0.45mol/(L·s),则所经历的时间是
2NH3的反应中,经过一段时间后,NH3的浓度增加0.6mol/L,在此时间内用H2表示的平均反应速率为0.45mol/(L·s),则所经历的时间是
 2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6 mol·L-1 。此时间内用H2表示的平均速率为0.45 mol·L-1·s-1,则此段时间值是
2NH3的反应中,经过一段时间后,NH3的浓度增加了0.6 mol·L-1 。此时间内用H2表示的平均速率为0.45 mol·L-1·s-1,则此段时间值是