题目内容
【题目】某温度时,使用一对石墨电极电解饱和Na2SO4溶液,当转移2 mol电子时停止电解,析出Na2SO4·10H2O晶体m g,所有数据都在相同温度下测得,下列叙述不正确的是
A. 电解后溶液质量减少(m+18)g
B. 原溶液中Na2SO4的质量分数为![]()
C. 若其他条件不变,将石墨替换为铜电极,则阴极析出1mol H2
D. 若其他条件不变,将石墨替换为铜电极,则析出Na2SO4·10H2O晶体仍为m g
【答案】D
【解析】本题考查的是电解原理,饱和溶液有关计算等知识点,为高频考点。侧重考查学生分析能力和计算能力,明确饱和溶液的特点,电解时阳极上铜失去电子而不是溶液中的阴离子失去电子是易错点。
A.电解后溶液质量减少量=电解水的质量+析出晶体的质量=(18+m)g,故正确;B.析出硫酸钠的质量为![]() =71/161mg,溶液质量=(18+m)g,溶液质量分数=溶质质量/溶液质量=
=71/161mg,溶液质量=(18+m)g,溶液质量分数=溶质质量/溶液质量= 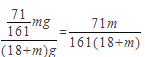 ,故正确;C. 若气体条件不变,将石墨电极替换为铜电极,阴极上仍然是氢离子放电生成氢气,但是阳极上铜失去电子生成铜离子,阴极上析出1mol氢气,故错误;D若其它条件不变,将石墨电极替换为铜电极,阳极上生成铜离子,阴极上生成氢气同时还有氢氧根离子生成,铜离子和氢氧根离子反应生成氢氧化铜沉淀,其电池反应为Cu+2H2O
,故正确;C. 若气体条件不变,将石墨电极替换为铜电极,阴极上仍然是氢离子放电生成氢气,但是阳极上铜失去电子生成铜离子,阴极上析出1mol氢气,故错误;D若其它条件不变,将石墨电极替换为铜电极,阳极上生成铜离子,阴极上生成氢气同时还有氢氧根离子生成,铜离子和氢氧根离子反应生成氢氧化铜沉淀,其电池反应为Cu+2H2O![]() Cu(OH)2+H2↑,根据方程式可知,转移2mol电子,消耗2mol水,则析出Na2SO4·10H2O晶体为2mg,故错误。故选D。
Cu(OH)2+H2↑,根据方程式可知,转移2mol电子,消耗2mol水,则析出Na2SO4·10H2O晶体为2mg,故错误。故选D。

【题目】下列有关实验操作、现象和解释或结论有错误的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 少量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B |
| 左边棉球变为橙色,右边棉球变为蓝色 | 证明氧化性:Cl2>Br2,但不能证明氧化性:Br2>I2 |
C | 向某溶液中加入硝酸银溶液 | 产生白色沉淀 | 则溶液有氯离子 |
D | 浓HNO3加热 | 有红棕色气体产生 | HNO3有不稳定性 |
A. AB. BC. CD. D
【题目】一氧化氮、二氧化氮等氮氧化物是常见的大气污染物,然而它们在工业上有着广泛的用途。
已知:①室温下,2NO+Na2O2=2NaNO2;②酸性条件下,NO或NO2-都能与MnO4—反应生成NO3-。
Ⅰ.以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示:
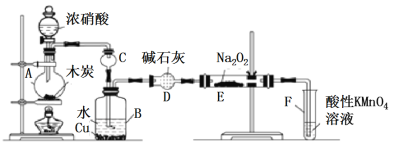
(1)A中反应的化学方程式_____________;
(2)装置B中观察到的主要现象______________;
(3)仪器D的名称是___________________;
(4)A中滴入浓硝酸之前,应先通入N2一段时间,原因是____________;
(5)写出NO被酸性KMnO4氧化的离子反应方程式______________;
(6)若无装置D,则E中产物除NaNO2外,还有_______(填化学式)。
Ⅱ.某研究性学习小组对NO2与Na2O2能否发生反应进行探究。
步骤1:提出假设
假设一:NO2与Na2O2不反应;
假设二:NO2能被Na2O2氧化;
假设三:______________________________________________。
步骤2:设计实验
(1)实验时,将NO2气体通入盛有Na2O2的玻璃管中,淡黄色粉末完全变成白色,说明假设________不成立。
(2)为验证假设二是否成立,该小组同学进行如下定性实验研究,请完成下表内容。
实验步骤(不要求写具体操作过程,试剂、仪器任选) | 预期的实验现象及结论 |
取适量的白色固体置于试管中,加蒸馏水溶解, ①__________________________________________ | ②___________________________ |