题目内容
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成能使湿润红色石蕊试纸变蓝的气体XZ3.请回答:(1)X元素的单质在自然界中 (填“能”或“不能”)稳定存在,写出该单质分子的结构式
(2)X的最高价氧化物对应水化物分子式是 ,XZ3的电子式是
(3)写出将XZ3通入稀盐酸中的反应方程式
(4)已知X和Y形成的一种化合物中X、Y分别显最低和最高价,则其化学式 ,若该物质熔点很高,推测该化合物属于 晶体.
【答案】分析:短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,则有两种元素在第二周期,有一种元素在第一周期,Z应为H元素,
Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y应为C元素,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X应为N元素,X和Z可以形成能使湿润红色石蕊试纸变蓝的气体XZ3,为NH3,结合对应原子的结构以及单质、化合物的性质解答该题.
解答:解:短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,则有两种元素在第二周期,有一种元素在第一周期,Z应为H元素,Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y应为C元素,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X应为N元素,
则X为N,Y为C,Z为H,
(1)X对应的单质为N2,在自然界中能以单质的形成存在,结构式为N≡N,故答案为:能;N≡N;
(2)X为N,对应的最高价氧化物对应水化物为HNO3,XZ3为NH3,电子式为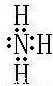 ,故答案为:HNO3;
,故答案为:HNO3;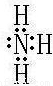 ;
;
(3)NH3通入盐酸中发生反应:NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
(4)N和C形成的一种化合物中N、C分别显最低和最高价,则其化学式为C3N4,由于熔点高,应为原子晶体,
故答案为:C3N4;原子.
点评:本题考查原子的结构与元素周期律的关系,题目难度中等,本题侧重于原子结构与对应化合物的结构和性质的考查,解答时注意原子的结构特点,为解答该题的关键.
Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y应为C元素,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X应为N元素,X和Z可以形成能使湿润红色石蕊试纸变蓝的气体XZ3,为NH3,结合对应原子的结构以及单质、化合物的性质解答该题.
解答:解:短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,则有两种元素在第二周期,有一种元素在第一周期,Z应为H元素,Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y应为C元素,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X应为N元素,
则X为N,Y为C,Z为H,
(1)X对应的单质为N2,在自然界中能以单质的形成存在,结构式为N≡N,故答案为:能;N≡N;
(2)X为N,对应的最高价氧化物对应水化物为HNO3,XZ3为NH3,电子式为
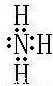 ,故答案为:HNO3;
,故答案为:HNO3;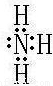 ;
;(3)NH3通入盐酸中发生反应:NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
(4)N和C形成的一种化合物中N、C分别显最低和最高价,则其化学式为C3N4,由于熔点高,应为原子晶体,
故答案为:C3N4;原子.
点评:本题考查原子的结构与元素周期律的关系,题目难度中等,本题侧重于原子结构与对应化合物的结构和性质的考查,解答时注意原子的结构特点,为解答该题的关键.

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目



