题目内容
2000年,河南发现世界级特大金红石(含TiO2)矿床。钛和钛合金及其重要化合物,在许多领域具有广泛、重要的应用,被称为21世纪的金属。(1)钛元素的同位素有:![]() 、
、![]() 、
、![]() 、
、![]() ,则下列说法正确的是( )
,则下列说法正确的是( )
A.可计算出钛元素的相对原子质量为48
B.钛元素的五种同位素化学性质均不相同
C.钛元素在元素周期表中位于第四周期
D.钛与铁(26Fe)同为第Ⅷ族元素
(2)TiO2(二氧化钛)是高级的白色颜料,它可用下列反应制得:
第一步:FeTiO3+2H2SO4====TiOSO4+FeSO4+2H2O,此时钛铁矿中的Fe2O3也与H2SO4发生反应,可加入铁屑使其还原成Fe2+,写出此过程的离子反应方程式:____________________。
第二步:TiOSO4+2H2O![]() TiO2·H2O+H2SO4-Q,制二氧化钛的关键是第二步水解反应。为使第二步反应进行得更完全,可采用下列_______措施。
TiO2·H2O+H2SO4-Q,制二氧化钛的关键是第二步水解反应。为使第二步反应进行得更完全,可采用下列_______措施。
A.加酸 B.加碱 C.加热 D.加压
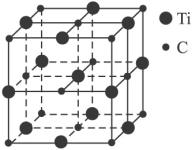
(3)最近发现一种由钛原子和碳原子构成的气态团簇分子,如图所示,则它的化学式为_________。
解析:(1)由各同位素的质量数可求出元素的近似相对原子质量,但还要知道其各自的百分含量;同种元素的不同同位素化学性质相同;钛位于第四周期ⅣB族。
(2)由平衡移动的原理可选出B、C。
(3)由于此物质是气态团簇分子,只需数出构成该分子的原子的个数,即Ti13C14。
答案:(1)C
(2)Fe2O3+6H++Fe====3Fe2++3H2O BC
(3)Ti13C14

练习册系列答案
 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
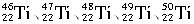 ,则下列说法正确的是 ()。
,则下列说法正确的是 ()。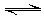 TiO2?H2O+H2SO4,正反应为吸热反应。
TiO2?H2O+H2SO4,正反应为吸热反应。