题目内容
aXn-和bYm+为短周期两元素的离子,它们的电子层结构相同,下列判断错误的是( )
| A、原子半径X<Y |
| B、X的气态氢化物的化学式为HnX或XHn |
| C、a+n=b-m |
| D、Y的最高价氧化物的化学式为YOm |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:aXn-和bYm+为短周期两元素的离子,它们的电子层结构相同,则a+n=b-m,且Y位于X下一周期,原子序数Y>X,且X为非金属元素、Y为金属元素,再结合题目分析解答.
解答:
解:aXn-和bYm+为短周期两元素的离子,它们的电子层结构相同,则a+n=b-m,且Y位于X下一周期,原子序数Y>X,且X为非金属元素、Y为金属元素,
A.电子层数越多其原子半径越大,所以原子半径Y>X,故A正确;
B.X元素的负化合价为-n,根据化合物中各元素化合价的代数和为0知,X氢化物的化学式为HnX或XHn,故B正确;
C.电子层结构相同的离子,其核外电子数相等,所以a+n=b-m,故C正确;
D.Y元素的最高正价为m价,Y的最高价氧化物的化学式为Y2Om或YO,故D错误;
故选D.
A.电子层数越多其原子半径越大,所以原子半径Y>X,故A正确;
B.X元素的负化合价为-n,根据化合物中各元素化合价的代数和为0知,X氢化物的化学式为HnX或XHn,故B正确;
C.电子层结构相同的离子,其核外电子数相等,所以a+n=b-m,故C正确;
D.Y元素的最高正价为m价,Y的最高价氧化物的化学式为Y2Om或YO,故D错误;
故选D.
点评:本题考查了原子结构和元素周期律,根据离子电子层结构确定两种元素核外电子数的关系及元素在周期表中的位置,再结合元素周期律解答,易错选项是D,注意如果m为2时的情况,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
下列说法正确的是( )
| A、2013年1月1日起,我省正式发布环境空气质量指数(AQI),包括PM2.5、PM10、O3、CO2、SO2和NO2等6项指标 |
| B、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C、明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 |
| D、将实验室的废酸液和废碱液中和后再排放符合“绿色化学”的要求 |
分类是化学学习与研究的常用方法,下列分类正确的是( )
| A、根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质 |
| B、石灰石、生石灰、熟石灰均属于碱 |
| C、根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| D、Na2O、MgO、Al2O3均属于碱性氧化物 |
把一小块镁、铝合金放入6mol?L-l的NaOH溶液中,可以形成微型原电池.则该电池负极上发生的电极反应为( )
| A、Mg-2e-═Mg2+ |
| B、A1+4OH--3e-═AlO2-+2H2O |
| C、4OH--4e-═2H2O+O2↑ |
| D、2H2O+2e-═2OH-+H2↑ |
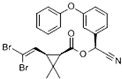 拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是( )| A、属于芳香烃 |
| B、属于卤代烃 |
| C、属于高分子化合物 |
| D、属于有机化合物 |
下列设备工作时,将化学能转化为热能的是( )
A、 太阳能集热器 |
B、 硅太阳能电池 |
C、 燃气灶 |
D、 锂离子电池 |