题目内容
实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡。将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口。静置、冷却一段时间后收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:__________________________________。
(2)采用水浴加热的原因是__________________________________________________。
(3)反应时铁屑过量的目的是(用离子方程式表示)____________________________。
(4)溶液趁热过滤的原因是__________________________________________________。
(5)塞紧试管口的目的是____________________________________________________。
(6)静置冷却一段时间后,在试管中观察到的现象是____________________________。
(1)写出该实验制备硫酸亚铁的化学方程式:__________________________________。
(2)采用水浴加热的原因是__________________________________________________。
(3)反应时铁屑过量的目的是(用离子方程式表示)____________________________。
(4)溶液趁热过滤的原因是__________________________________________________。
(5)塞紧试管口的目的是____________________________________________________。
(6)静置冷却一段时间后,在试管中观察到的现象是____________________________。
(1)Fe + H2SO4=FeSO4 +H2↑(2)水浴加热受热均匀,温度容易控制。
(3)Fe+2Fe3+=3Fe2+(4)溶液趁热过滤的目的是减少FeSO4的损失;
(5)防止空气中的氧气将FeSO4氧化。(6)有浅绿色硫酸亚铁晶体析出
(3)Fe+2Fe3+=3Fe2+(4)溶液趁热过滤的目的是减少FeSO4的损失;
(5)防止空气中的氧气将FeSO4氧化。(6)有浅绿色硫酸亚铁晶体析出
试题分析:(1)铁是活泼的金属和稀硫酸反应生成硫酸亚铁,反应的化学方程式是Fe + H2SO4=FeSO4 +H2↑。
(2)采用水浴加热能使溶液受热均匀,且温度容易控制。
(3)硫酸亚铁易被氧化生成硫酸铁,所以反应时铁屑过量的目的是防止硫酸亚铁被氧化,反应的离子方程式是Fe+2Fe3+=3Fe2+。
(4)因为一般物质的溶解度随温度的升高而增大,所以溶液趁热过滤的目的是减少FeSO4的损失。
(5)由于硫酸亚铁易被氧化生成硫酸铁,所以塞紧试管口的目的是防止空气中的氧气将FeSO4氧化。
(6)硫酸亚铁晶体是显浅绿色的,所以一段时间后在试管中观察到的现象是有浅绿色硫酸亚铁晶体析出。
点评:该题是高考中的常见题型,属于中等难度的试题。试题通过硫酸亚铁的制备,重点考查学生对实验原理、实验设计以及实验操作能力的培养,有利于调动学生的学习兴趣,激发学生的学习积极性。该题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
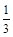 体积的自来水,并放入几粒沸石
体积的自来水,并放入几粒沸石