题目内容
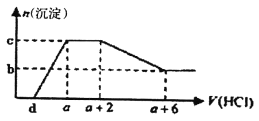
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是
A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
【答案】C
【解析】由图象分析可知,开始无沉淀生成说明加入的盐酸和溶液中的碱反应,说明溶液中一定含OH-离子,则与氢氧根离子不能共存的是Fe3+、Mg2+、Al3+;随后反应生成沉淀逐渐增大,说明是AlO2-、SiO32-和氢离子反应生成氢氧化铝沉淀和硅酸沉淀,由于AlO2-与HCO3-发生反应生成氢氧化铝沉淀,则溶液中一定不存在HCO3-;继续加入盐酸沉淀量不变,消耗盐酸的离子只能是CO32-离子,反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐酸,最后剩余沉淀为硅酸;硫酸根离子不能确定是否存在,但根据溶液的电中性可知,溶液中一定含有Na+离子。A.溶液中硫酸根离子不能确定,剩余原溶液中不一定含有Na2SO4,故A错误;B.依据判断原溶液中一定含有的阴离子是:OH-、SiO32-、AlO2-、CO32-,故B错误;C.依据图像可知和碳酸根离子反应的盐酸为2体积,CO32-+2H+=CO2↑+H2O 氢氧化铝溶解消耗的盐酸体积为4体积,Al(OH)3+3H+=Al3++3H2O,原溶液中含有CO32-与AlO2-的物质的量之比为3:4,故C正确;D.根据图像溶解氢氧化铝消耗的盐酸体积为4,假设盐酸的浓度为1mol/L,则消耗氯化氢4mol,则溶解的氢氧化铝为![]() mol,则溶液中含有
mol,则溶液中含有![]() mol AlO2-,沉淀
mol AlO2-,沉淀![]() mol AlO2-需要盐酸
mol AlO2-需要盐酸![]() mol,a-d对应于AlO2-和SiO32-消耗的盐酸大于
mol,a-d对应于AlO2-和SiO32-消耗的盐酸大于![]() mol,即a-d>
mol,即a-d>![]() ,故D错误;故选C。
,故D错误;故选C。

【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)








