题目内容
在某l00mL混合溶液中,HNO3和H2SO4的物质的量浓度分别为0.4 mol/L和0.1 mol/L,向该混合溶液中加入l.92g铜粉,加热,充分反应后,所得的Cu2+的物质的量浓度为
| A.0.15 mol/L | B.0.225 mol/L | C.0.35 mol/L | D.0.45 mol/L |
B
从浓度上判断该题的硝酸和硫酸属于稀酸,稀硝酸与铜反应放出NO,而硫酸的作用在于提供H+,通过计算得出硝酸物质的量为0.04mol,硫酸物质的量为0.01mol,铜有0.03mol.很明显,氢离子总物质的量为0.04+0.01×2=0.06mol,硝酸根离子有0.04mol而铜却有0.03mol.在知晓这些基本情况下,列出离子反应方程:
3Cu+8H++2NO3—=3Cu2++2NO+4H2O。观察得出将铜反应完需要0.08mol的氢离子和0.02mol的硝酸根离子.现在硝酸根离子是够反应的,氢离子的量不够,反应中氢离子被消耗干净,硝酸根不再表现氧化性,反应停止,铜有剩余.所以该题的关键就应以氢离子的量来进行计算.
假设铜离子的物质的量为X,根据关系式:8H+~3Cu2+可得出:
X=0.06÷8×3=0.0225mol 浓度=0.0225mol÷0.1L=0.225mol/L
3Cu+8H++2NO3—=3Cu2++2NO+4H2O。观察得出将铜反应完需要0.08mol的氢离子和0.02mol的硝酸根离子.现在硝酸根离子是够反应的,氢离子的量不够,反应中氢离子被消耗干净,硝酸根不再表现氧化性,反应停止,铜有剩余.所以该题的关键就应以氢离子的量来进行计算.
假设铜离子的物质的量为X,根据关系式:8H+~3Cu2+可得出:
X=0.06÷8×3=0.0225mol 浓度=0.0225mol÷0.1L=0.225mol/L

练习册系列答案
相关题目
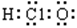
 2H++S2-
2H++S2-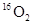 和1.12L
和1.12L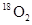 均含有0.1
均含有0.1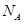 个氧原子
个氧原子