题目内容
【题目】据报道,科学家新合成了一种抗癌、治癌的药物,其化学式可表示为10B20 . 下列叙述正确的是( )
A.10B20为硼元素的一种原子
B.10B20为硼元素的一种单质
C.10B20的中子数比核外电子数多
D.10B20的原子核外电子排布为 
【答案】B
【解析】解:A、10B20是由20个10B原子组成的分子,故A错误;
B、10B20是由B元素组成的单质,一个10B20分子由20个10B构成,故B正确;
C、10B的中子数=10﹣5=5,核外电子数=质子数=5,故C错误;
D、10B20的原子核外电子排布为 ![]() ,故D错误;
,故D错误;
故选B.
【考点精析】关于本题考查的核素和质量数与质子数、中子数之间的相互关系,需要了解核素符号:如2713Al、3216S、168O左上角为质量数,左下角为质子数;A=N+Z(A:质量数,N:中子数,Z:质子数)才能得出正确答案.

 名校课堂系列答案
名校课堂系列答案【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2。该反应的还原产物为______。
(2)已知反应2HI(g)![]() H2(g)+I2(g)的△H = +11 kJ·mol-1,l molH2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(s)分子中化学键断裂时需吸收的能量为______kJ。
H2(g)+I2(g)的△H = +11 kJ·mol-1,l molH2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(s)分子中化学键断裂时需吸收的能量为______kJ。
(3)Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g)。在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)。在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为__________________。
②上述反应中,正反应速率为![]() 正=k正x2(HI),逆反应速率为
正=k正x2(HI),逆反应速率为![]() 逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为____________________(以K和k正表示)。若k正=0.0027 min-1,在t = 40 min时,
逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为____________________(以K和k正表示)。若k正=0.0027 min-1,在t = 40 min时, ![]() 正 = _______________min-1。
正 = _______________min-1。
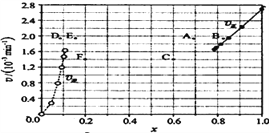
③由上述实验数据计算得到![]() 正~x(HI)和
正~x(HI)和![]() 逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。
逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为______________(填字母)。