题目内容
(6分)有0.1mol某有机物和0.25mol氧气在一密闭容器中燃烧,所得气体产物为CO2、CO、H2O(气),产物依次通过浓硫酸时,浓硫酸质量增加了5.4g,再通过炽热的氧化铜时,氧化铜质量减轻了1.6g,最后通过碱石灰时,碱石灰的质量增加了8.8g。
(1)求该有机物的分子式。(请写出计算过程)
(2)写出其可能的结构简式。
(1)求该有机物的分子式。(请写出计算过程)
(2)写出其可能的结构简式。
(6分)分子式:C2H6O 结构简式为:CH3CH2OH CH3OCH3
浓硫酸质量增加了5.4g,说明生成的水蒸气为0.3mol;

可知,生成的气体产物中含有0.1molCO,同时生成了0.1molCO2;
通过碱石灰时,碱石灰的质量增加了8.8g,说明CO2气体为0.2mol,则原气体产物中CO2为0.1mol
根据原子守恒可知,0.1mol该有机物中含有的碳原子为0.2mol,氢原子为0.6mol,氧原子为0.1mol,故该有机物的分子式为C2H6O,可能的结构为CH3CH2OH CH3OCH3

可知,生成的气体产物中含有0.1molCO,同时生成了0.1molCO2;
通过碱石灰时,碱石灰的质量增加了8.8g,说明CO2气体为0.2mol,则原气体产物中CO2为0.1mol
根据原子守恒可知,0.1mol该有机物中含有的碳原子为0.2mol,氢原子为0.6mol,氧原子为0.1mol,故该有机物的分子式为C2H6O,可能的结构为CH3CH2OH CH3OCH3

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目

 ”不稳定)。
”不稳定)。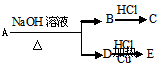
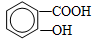
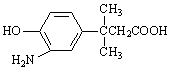 的表述不正确的是
的表述不正确的是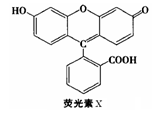
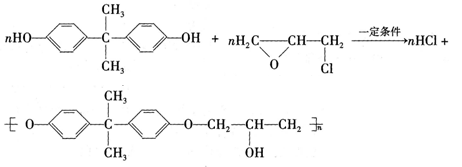
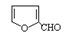 )发生缩聚反应
)发生缩聚反应 若此有机物跟FeCl3溶液作用显紫色,其一溴代物共有三种同分异构,写出此有机物的结构简式。
若此有机物跟FeCl3溶液作用显紫色,其一溴代物共有三种同分异构,写出此有机物的结构简式。