题目内容
【题目】将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
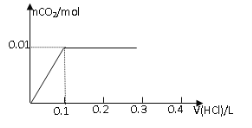
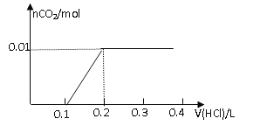
A B
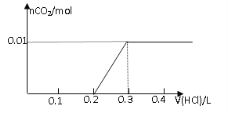
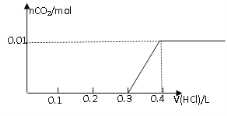
C D
【答案】D
【解析】
试题分析:对NaOH和Na2CO3混合配成的溶液,当滴加盐酸时,先发生氢氧化钠与盐酸的中和反应,再发生碳酸钠与盐酸的反应生成碳酸氢钠和氯化钠,最后发生碳酸氢钠与盐酸反应才有二氧化碳气体生成,有关反应的方程式分别是NaOH+HCl=NaCl+H2O、HCl+Na2CO3=NaHCO3+NaCl、NaHCO3+HCl=NaCl+H2O+CO2↑。0.8g NaOH和1.06g Na2CO3物质的量分别是0.8g÷40g/mol=0.02mol、1.06g÷106/mol=0.01mol,三步反应中消耗氯化氢的物质的量分别是0.02mol、0.01mol和0.01mol,对应盐酸的体积是0.2L、0.1L、0.1L,即盐酸的体积滴加到0.3L时开始出现气体,滴加到0.4L时气体达到最大值,因此选项D符合,答案选D。

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案 名题金卷系列答案
名题金卷系列答案
相关题目




