题目内容
下列反应的离子方程式正确的是
| A.Na2CO3溶液与NaHSO4溶液反应:CO32--+2H+=CO2↑+H2O |
| B.向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ |
| C.碘化钾溶液中滴入稀硫酸酸化的双氧水反应:2I-+H2O2+2H+=H2O+I2 |
| D.海水制取溴时用纯碱吸收吹出的溴:3Br2+3H2O=5Br-+BrO3-+6H+ |
A
解析

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
某溶液中可能含有以下6种离子中的几种:NH4+、A13+、Mg2+、CO32―、Cl一、SO42―,为确认溶液组成,现取100 mL分成三等份溶液进行如下实验:
(1)向第一份溶液中加入 AgNO3溶液有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液充分反应后,最终得到沉淀0.58 g,同时收集到气体0.03 mol(设气体全部从溶液中逸出);
(3)向第三份溶液中加入足量BaCl2溶液(盐酸酸化)充分反应后,得到沉淀6.99 g。
由此可知,下列关于原溶液组成的正确结论是( )
| A.一定存在Cl一 |
| B.溶液中含有A13+和NH4+ |
| C.一定不存在Mg2+,可能存在A13+ |
| D.溶液中SO42―的浓度是0. 3 mol/L |
下列离子方程式不正确的是
| A.向AgCl悬浊液中加入Na2S溶液:2AgCl+S2-=Ag2S+2Cl- |
| B.向NaHCO3溶液中加入NaOH溶液:HCO3-+OH-= CO32-+H2O |
| C.向Ba(OH)2溶液中加入稀H2SO4:Ba2++OH-+H++ SO42-= BaSO4↓+ H2O |
| D.向Cu粉中加入过量的浓HNO3:Cu+4 H++ 2NO3-= Cu2++2 NO2↑+2H2O |
某无色溶液中存在大量的H+、NH4+、SO42-,该溶液中还可能存在的离子是
| A.K+ | B.Ba2+ | C.OH- | D.HCO3- |
向硫酸铝铵溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.NH4+ + SO42—+ Ba2+ +OH— BaSO4↓+ NH3·H2O BaSO4↓+ NH3·H2O |
B.2Al3+ + 3SO42—+3Ba2+ +6OH— 3BaSO4↓+ 2Al(OH)3↓ 3BaSO4↓+ 2Al(OH)3↓ |
C.Al3+ + 2SO42—+ 2Ba2+ + 4OH— 2BaSO4↓+ AlO2—+ 2H2O 2BaSO4↓+ AlO2—+ 2H2O |
D.NH4++Al3+ +2SO42—+2Ba2+ +4OH— 2BaSO4↓+ Al(OH)3↓+ NH3·H2O 2BaSO4↓+ Al(OH)3↓+ NH3·H2O |
下列离子方程式正确的是
A.将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++ +OH-=== CaCO3↓+H2O +OH-=== CaCO3↓+H2O |
| B.三氯化铁溶液中通入硫化氢气体:2Fe3++3H2S===Fe2S3↓+6H+ |
C.用稀硝酸浸泡做过银镜反应的试管:Ag+2H++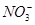 ===Ag++NO2↑+H2O ===Ag++NO2↑+H2O |
D.4 mol·L-1的NaAlO2溶液和7 mol·L-1的HCl等体积互相均匀混合:4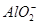 + 7H++ H2O===3Al(OH)3↓+ Al3+ + 7H++ H2O===3Al(OH)3↓+ Al3+ |
下列各溶液中能大量共存的离子组是( )
| A.c(H+)=10-14 mol·L-1的溶液中:Na+、AlO2-、S2-、SO32- |
| B.使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C.碳酸氢钠溶液中:K+、SO42-、Cl-、H+ |
| D.使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO42-、K+ |
下列离子方程式表达正确的是( )
| A.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| B.硫酸亚铁在空气中氧化:4Fe2++3O2+6H2O=4Fe(OH)3↓ |
| C.向氯化铝溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O |
| D.碳酸氢镁溶液中加入足量的NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
某同学为检验溶液中是否含有常见的几种无机离子,进行了如下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是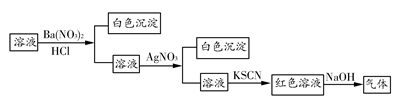
A.原溶液中一定含有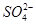 |
B.原溶液中一定含有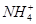 |
| C.原溶液中一定含有Cl- |
| D.原溶液中一定含有Fe3+ |